
Tóm tắt
Nội dung bài
Giảm tiểu cầu do thuốc (Drug-induced thrombocytopaenia)
Giảm tiểu cầu do thuốc là tình trạng phổ biến nhất trong số các rối loạn tiểu cầu do thuốc. Dựa trên cơ chế bệnh sinh, giảm tiểu cầu do thuốc có thể phân loại thành giảm tiểu cầu do thuốc qua miễn dịch (drug-induced immune thrombocytopaenia - DITP), giảm tiểu cầu không qua trung gian miễn dịch và giảm tiểu cầu do heparin (HIT). Giảm tiểu cầu thường đặc trưng bởi tình trạng số lượng tiểu cầu trong máu < 150 G/L. Triệu chứng lâm sàng của giảm tiểu cầu được quan sát thấy có thể từ mức độ nhẹ (như: ban xuất huyết dưới da, bầm tím, chảy máu niêm mạc) đến các biến chứng xuất huyết nghiêm trọng trên lâm sàng [1]. Giảm tiểu cầu là tác dụng không mong muốn đã được ghi nhận đối với nhiều loại thuốc và nhóm thuốc khác nhau. Đặc biệt, hơn 300 loại thuốc được chứng minh là có liên quan đến giảm tiểu cầu do thuốc thông qua miễn dịch [2]. Trong đó, một nghiên cứu tổng quan hệ thống ghi nhận các loại thuốc được báo cáo phổ biến nhất bao gồm heparin, quinin, quinidin, các kháng sinh (vancomycin, sulfamethoxazol/ trimethoprim, penicillin, ceftriaxon), rifampin, carbamazepin, ibuprofen, mirtazapin, oxaliplatin và eptifibatid [2].
Cơ chế giảm tiểu cầu do thuốc
Giảm tiểu cầu trong DITP là kết quả của sự phá hủy tiểu cầu do các kháng thể phụ thuộc thuốc (drug-dependent antibody - DDAbs) phản ứng với glycoprotein trên màng tiểu cầu [3]. Trong đó, các loại thuốc khác nhau thường thể hiện tác dụng này thông qua loại kháng thể phụ thuộc thuốc khác nhau như trình bày tại Bảng 1.
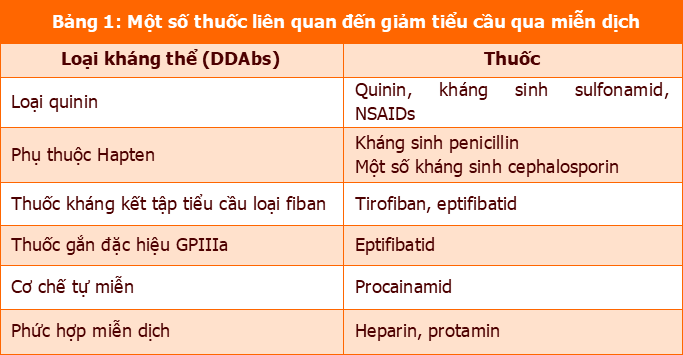
Ngược lại, cơ chế của giảm tiểu cầu do thuốc không qua trung gian miễn dịch là tác dụng gây độc tế bào trực tiếp của các phân tử thuốc lên tế bào tủy xương tạo máu và/hoặc tiểu cầu, dẫn đến rối loạn chức năng tạo tiểu cầu của tủy xương hoặc tăng phá hủy tiểu cầu trong tuần hoàn [3]. Ví dụ, các thuốc điều trị ung thư thường gây giảm tiểu cầu do gây độc trực tiếp tế bào gốc tạo máu [3]. Kháng sinh linezolid cũng gây giảm tiểu cầu thông qua ức chế tủy xương [4]. Ngoài ra, các thuốc lợi tiểu thiazid cũng liên quan đến biến cố giảm tiểu cầu không qua trung gian miễn dịch. Bên cạnh đó, một số thuốc (như tamoxifen, methotrexat, aspirin, vancomycin, cisplatin, lovastatin) cho thấy có tác dụng gây chết tiểu cầu theo chương trình (apoptosis). Tuy nhiên, ý nghĩa lâm sàng của biến cố giảm tiểu cầu dựa trên tác dụng này còn chưa rõ ràng [3], [5].
Giảm tiểu cầu do heparin có thể do 2 cơ chế bao gồm giảm tiểu cầu không do miễn dịch (HIT loại 1) và giảm tiểu cầu do miễn dịch (HIT loại 2). Cụ thể HIT loại 1 có thể xảy ra trên khoảng 10% đến 30% bệnh nhân được điều trị bằng heparin, trong khi, HIT loại 2 xuất hiện với tần xuất ít hơn. HIT loại 1 do heparin liên kết trực tiếp với tiểu cầu, dẫn đến hoạt hóa tiểu cầu ở mức độ nhẹ. Trong khi, cơ chế bệnh sinh của HIT loại 2 thông qua phản ứng của heparin với yếu tố tiểu cầu 4 (PF4) để tạo ra phức hợp miễn dịch đặc hiệu [3].
Biểu hiện lâm sàng/cận lâm sàng
DITP thường liên quan đến nguy cơ xuất hiện biến chứng xuất huyết cao. Một nghiên cứu về các trường hợp có biến cố DITP cho thấy tỷ lệ xuất huyết nghiêm trọng và tử vong chiếm lần lượt khoảng 9% và 0,8% [3]. Thời gian khởi phát thường xảy ra sau khoảng 5 đến 10 ngày kể từ khi sử dụng với thuốc, với ngưỡng tiểu cầu thấp nhất có thể < 20 G/L. Ngoài trừ, các trường hợp giảm tiểu cầu do thuốc đối kháng GPIIb/IIIa (eptifibatid, abciximab) thường xuất hiện sớm trong vòng vài giờ sau khi sử dụng thuốc [3]. Biện pháp xử trí DITP thường là ngừng thuốc nghi ngờ. Trong trường hợp dùng nhiều loại thuốc, cần ngừng tất cả các thuốc sử dụng trong vòng 2 tuần trước khi xuất hiện biến cố và cân nhắc thuốc thay thế phù hợp nếu cần thiết. Số lượng tiểu cầu thường bắt đầu hồi phục sau 4 đến 5 chu kỳ bán thải của thuốc hoặc chất chuyển hóa có khả năng gây giảm tiểu cầu. Lưu ý, biện pháp truyền tiểu cầu thường không hiệu quả khi các thuốc gây DITP còn trong huyết tương. Liều cao immunoglobulin tĩnh mạch (IVIG) có thể được dùng cho những bệnh nhân bị giảm tiểu cầu nặng và có xuất huyết nghiêm trọng hay ở bệnh nhân có nguy cơ chảy máu cao [1], [3].
Đối với giảm tiểu cầu do heparin, HIT được định nghĩa khi số lượng tiểu cầu giảm >50% so với giá trị cao nhất trước khi điều trị với heparin. HIT loại 1 thường xảy ra trong khoảng 5 ngày đầu tiên khi điều trị heparin. Mức độ giảm tiểu cầu thường nhẹ (số lượng tiểu cầu thường duy trì ở mức 80 - 100 G/L) và không có biến cố nghiêm trọng trên lâm sàng. Biến cố này có khả năng tự phục hồi trong vài ngày mà không cần dừng heparin [3]. Khác với loại 1, HIT loại 2 thường thời gian khởi phát muộn hơn thường từ 5 đến 10 ngày sau khi sử dụng heparin. Đáng chú ý, HIT loại 2 có thể liên quan đến biến chứng huyết khối. Đây là biến chứng nghiêm trọng nhất của HIT và góp phần gây bệnh tật và tử vong trên bệnh nhân [3]. Do đó, khi chẩn đoán giảm tiểu cầu do heparin loại 2 nên ngừng heparin và cân nhắc liệu pháp thay thế với các thuốc chống đông khác dựa trên tình hình lâm sàng, chức năng gan, thận của bệnh nhân [3].
Tăng tiểu cầu do thuốc (Drug induced thrombocytosis)
Tăng tiểu cầu do thuốc được phân loại là tình trạng tăng tiểu cầu thứ phát tương đối hiếm gặp, đáng lưu ý là, trên lâm sàng rất khó để chẩn đoán phân biệt với tình trạng tăng tiểu cầu do một số nguyên nhân phổ biến khác (như tình trạng nhiễm trùng, thiếu máu do thiếu sắt, bệnh ung thư, bệnh lý viêm mạn tính, …) [6]. Vì vậy, hầu hết các nghiên cứu về tăng tiểu cầu thường coi tăng tiểu cầu do thuốc như một loại tăng tiểu cầu thứ phát không rõ nguyên nhân với tỷ lệ xuất hiện dao động từ 2,2 - 9,7% do phụ thuộc vào định nghĩa về tăng tiểu cầu, các yếu tố nguy cơ thuộc về người bệnh trong mẫu nghiên cứu [6]. Năm 2012, Rose và cộng sự đã đánh giá và phân loại được biến cố tăng tiều cầu do thuốc, từ đó, ghi nhận rằng phản ứng này chiếm khoảng 3% tổng số trường hợp có tăng tiều cầu thứ phát [7]. Một nghiên cứu tổng quan được công bố năm 2019, cho thấy các tác nhân thường gây tăng tiểu cầu bao gồm các heparin trọng lượng phân tử thấp (LMWH), kháng sinh, clozapin, adrenalin, gemcitabin và alkaloid vinca [6]. Trong khi đó, năm 2024, Trung tâm DI & ADR Quốc gia đã ghi nhận 6 báo cáo về phản ứng tăng tiểu cầu do thuốc, liên quan đến ertapenem (2 báo cáo), meropenem (1 báo cáo), ceftazidim (2 báo cáo) và fluconazol (1 báo cáo).
Biểu hiện lâm sàng/cận lâm sàng
Tổ chức Y tế Thế giới (WHO) khuyến cáo ngưỡng chẩn đoán tăng tiểu cầu là ≥ 450 x109 tế bào/L [8]. Tăng tiểu cầu thứ phát (bao gồm tăng tiều cầu do thuốc) có thể hồi phục và ít nguy cơ biến chứng mạch máu hơn so với tăng tiểu cầu nguyên phát, bất kể mức độ tăng tiểu cầu. Năm 2019, một nghiên cứu tổng quan ghi nhận được 43 báo cáo ca bệnh và 8 chuỗi ca bệnh về tăng tiểu cầu do thuốc với trung vị thời gian số lượng tiều cầu đạt đỉnh là 13 ngày và thời gian hồi hồi phục là 14 ngày [6]. Hầu hết các trường hợp tăng tiểu cầu được ghi nhận không yêu cầu biện pháp điều trị can thiệp y tế khác mà tự hồi phục sau khi ngừng thuốc hoặc điều chỉnh liều thuốc [6]. Nghiên cứu này cũng ghi nhận rằng thời gian khởi phát và thời gian phục hồi của tăng tiểu cầu là có sự khác biệt tương đối lớn giữa các loại thuốc nghi ngờ khác nhau. Ngoài các thuốc được trình bày tại Bảng 2, các tài liệu y văn cũng ghi nhận được ít nhất một báo cáo mô tả biến cố tăng tiểu cầu liên quan đến các thuốc như cyclosporin, efalizumab, yếu tố kích thích dòng bạch cầu hạt (G-CSF), isotretinoin, leflunomid, methylphenidat, methotrexat, miconazol và các thuốc ức chế tyrosine kinase (erlotinib, ruxolitinib) [6].
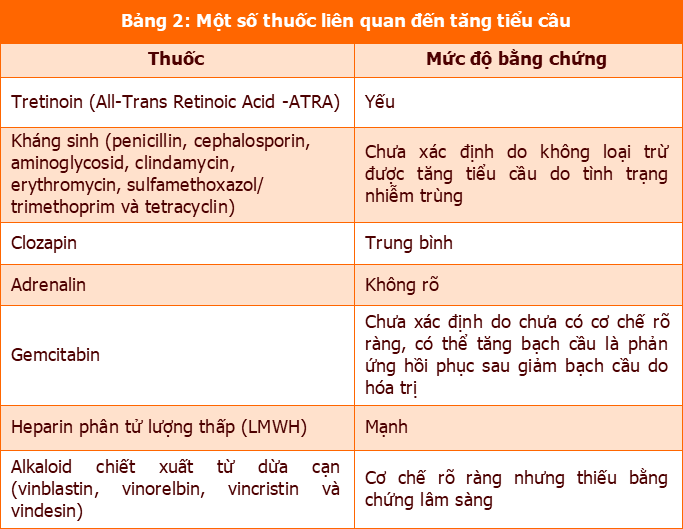
Cơ chế tăng tiểu cầu do thuốc
Cơ chế gây tăng tiểu cầu do thuốc hiện vẫn chưa rõ ràng. Tuy nhiên, cơ chế được đề xuất trong các tài liệu y văn hiện này bao gồm: (1) tăng sản xuất throbopoein, từ đó, kích thích sinh tế bào mẫu tiểu cầu (megakaryocyte) gây tăng sinh tiểu cầu; (2) tăng giải phóng interleukin (IL-6, IL-11) gây tăng sản xuất thrombopoietin thứ phát, dẫn đến tăng số lượng tiểu cầu [9].
Rối loạn chức năng tiểu cầu do thuốc (Drug-induced platelet dysfunction)
Khác với tăng tiểu cầu, thuốc được coi là căn nguyên chính gây tình trạng rối loạn chức năng tiểu cầu [10]. Một số thuốc như aspirin, clopidogrel, thuốc chẹn thụ thể (GPIIb-IIIa) đã được biết đến rộng rãi với tác dụng chống kết tập tiểu cầu. Ngoài ra, biến cố bất lợi này cũng đã được ghi nhận đối với một số thuốc khác trong nhóm kháng sinh beta-lactam, thuốc tim mạch hay các thuốc tác dụng trên hệ thần kinh trung ương [10].
Cơ chế rối loạn chức năng tiểu cầu do thuốc
Các thuốc khác nhau gây rối loạn chức năng tiểu cầu theo cơ chế khác nhau. Đối với các nhóm thuốc chống kết tập tiểu cầu, ảnh hưởng lên chức năng tiểu cầu thường thường là tác dụng dược lý mong muốn của các thuốc đó [11]. Cụ thể, aspirin (ASA) ức chế quá trình hình thành thromboxan A₂ (TXA2), trong khi, clopidogrel và ticagrelor đối kháng trực tiếp thụ thể P2Y12 trên màng tiểu cầu, dẫn đến ức chế quá trình hoạt hóa tiểu cầu. Ngoài ra, eptifibatid chống kết tập tiểu cầu thông qua ức chế thụ thể glycoprotein IIb/IIIa (GP IIb/IIIa) trên bề mặt tiểu cầu, ngăn cản quá trình kết tập và hình thành nút tiểu cầu [11]. Ngược lại, rối loạn chức năng tiểu cầu do các nhóm thuốc khác (như: kháng sinh beta-lactam, thuốc tim mạch, các thuốc tác dụng trên hệ thần kinh trung ương) lại là tác dụng không mong muốn của các nhóm thuốc này với cơ chế chưa rõ ràng [10]. Ý nghĩa trên lâm sàng và cơ chế được đề xuất của một số thuốc, nhóm thuốc gây rối loạn chức năng tiểu cầu được trình bày tại Bảng 3.
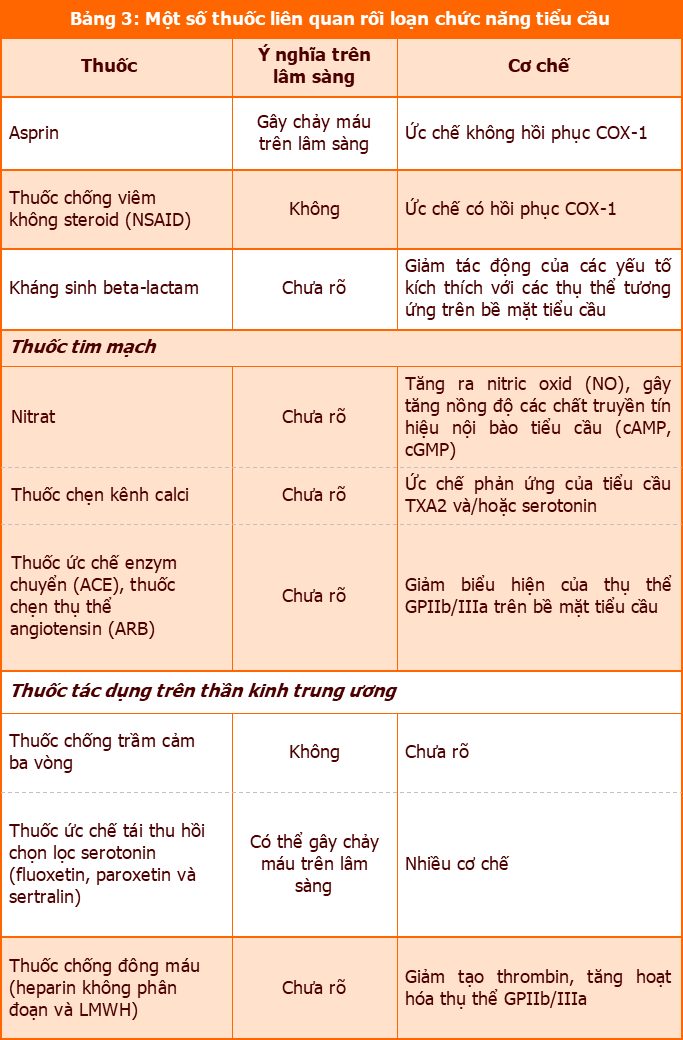
Biểu hiện lâm sàng/cận lâm sàng
Về cận lâm sàng, kết quả xét nghiệm bất thường về chức năng tiểu cầu hoặc thời gian chảy máu đã được ghi nhận đối với nhiều thuốc và nhóm thuốc như: aspirin, NSAID, kháng sinh penicillin, cephalosporin, các nhóm thuốc tim mạch, các statin, thuốc chống đông, thuốc ức chế tái thu hồi chọn lọc serotonin (SSRI). Tuy nhiên, hiện chỉ có aspirin và các thuốc nhóm SSRI đã được xác định có liên quan đến biến cố chảy máu trên lâm sàng [10]. Với aspirin, ức chế chức năng tiểu cầu do asprin thường khởi phát nhanh trong vòng 60 phút sau khi sử dụng thuốc. Tác dụng ức chế không hồi phục mà kéo dài suốt vòng đời của tiểu cầu (khoảng 8 -10 ngày) [12]. Bên cạnh đó, các nghiên cứu cũng đã ghi nhận tỷ lệ cao hơn của các tình trạng như xuất huyết tiêu hóa hay chảy máu trong máu trong phẫu thuật ở bệnh nhân sử dụng các thuốc ức chế tái thu hồi chọn lọc serotonin (SSRI) [10]. Do đó, việc sử dụng đồng thời aspirin hoặc các thuốc chống viêm không steroid (NSAIDs) với SSRI gây tăng đáng kể nguy cơ xuất huyết tiêu hóa, đặc biệt trên bệnh nhân cao tuổi [10]. Rối loạn chức năng tiểu cầu do thuốc gây ra thường nhẹ, một số triệu chứng lâm sàng thường gặp như dễ bầm tím, chảy máu cam, ban xuất huyết, xuất huyết tiêu hóa đã được ghi nhận khi sử dụng aspirin hay các SSRI [10], [13]. Một số xét nghiệm cận lâm sàng như thời gian chảy máu, xét nghiệm chức năng tiểu cầu PFA-100 có thể sử dụng để chẩn đoán xác định tình trạng này. Ngoài ra, trên lâm sàng một số yếu tố nguy cơ liên quan đến rối loạn tiểu cầu cần lưu ý như bệnh lý mắc kèm (bệnh lý gan mạn tính, suy thận, …), đang sử dụng đồng thời các thuốc (kháng virus, kháng sinh, thuốc chống đông) [10].
Biện pháp xử trí
Biến cố rối loạn tiểu cầu liên quan đến thuốc thường biểu hiện bởi các tình trạng xuất huyết mức độ nhẹ và ít ảnh hưởng đến lâm sàng trên bệnh nhân. Tuy nhiên, cần đánh giá các vấn đề liên quan biến cố bất lợi này (bao gồm sự cần thiết của thuốc nghi ngờ, mối quan hệ thuốc – ADR, tiền sử bệnh lý, tiền sử sử dụng thuốc) để giảm thiểu tỷ lệ xuất huyết trên bệnh nhân [10]. Đa số các biến cố xuất huyết mức độ nhẹ khi sử dụng các thuốc kháng tiểu cầu sẽ cải thiện sau khi ngừng thuốc. Một số ít trường hợp xuất huyết nghiêm trọng có thể cần truyền tiểu cầu cấp cứu. Việc ngừng điều trị thuốc nghi ngờ hay truyền tiểu cầu đều cần dựa trên đánh giá cẩn thận lợi ích và nguy cơ huyết khối trên từng cá thể người bệnh [14].
Kết luận
Biến cố rối loạn tiểu cầu (bao gồm tăng/giảm số lượng tiểu cầu, rối loạn chức năng tiểu cầu) đã được ghi nhận liên quan đến nhiều thuốc và nhóm thuốc khác nhau. Giảm tiểu cầu do thuốc là phản ứng phổ biến nhất, đồng thời, dữ liệu báo cáo ADR và y văn hiện nay đều đã ghi nhận tương đối rõ ràng và đầy đủ về phản ứng có hại này. Trong đó, các thuốc gây giảm tiểu cầu phổ biến nhất như heparin, thuốc điều trị ung thư, kháng sinh. Với tăng tiểu cầu và rối loạn chức năng tiểu cầu, tổng quan các tài liệu y văn cho thấy chỉ một số ít các thuốc, nhóm thuốc nghi ngờ có cơ chế rõ ràng và bằng chứng lâm sàng đầy đủ. Cụ thể, LMWH gây phản ứng tăng tiểu cầu với mức độ bằng chứng mạnh, trong khi, mức độ bằng chứng yếu hơn được ghi nhận đối với một số thuốc như clozapin, tretinoin. Đối với tình trạng rối loạn tiểu cầu do thuốc, chỉ asprin và các thuốc SSRI được chứng minh là liên quan đến biến cố xuất huyết có ý nghĩa lâm sàng. Do đó, các tình trạng rối loạn tiểu cầu trong thực tế lâm sàng cần được đánh giá một cách thận trọng, từ đó đưa ra các biện pháp xử trí phù hợp cho người bệnh.
Tài liệu tham khảo
1. Wolters Kluwer. Drug-induced immune thrombocytopenia. Uptodate [accessed 04/05/2025].
2. Arnold DM, Kukaswadia S, Nazi I, Esmail A, Dewar L, Smith JW, et al. A systematic evaluation of laboratory testing for drug-induced immune thrombocytopenia. J Thromb Haemost. 2013;11(1):169-76.
3. Bakchoul T, Marini I. Drug associated thrombocytopenia. Hematology Am Soc Hematol Educ Program. 2018;2018(1):576-83.
4. Cossu AP, Musu M, Mura P, De Giudici LM, Finco G. Linezolid-induced thrombocytopenia in impaired renal function: is it time for a dose adjustment? A case report and review of literature. Eur J Clin Pharmacol. 2014;70(1):23-8.
5. Towhid ST, Tolios A, Münzer P, Schmidt EM, Borst O, Gawaz M, et al. Stimulation of platelet apoptosis by balhimycin. Biochem Biophys Res Commun. 2013;435(2):323-6.
6. Vo QT, Thompson DF. A Review and Assessment of Drug-Induced Thrombocytosis. Ann Pharmacother. 2019;53(5):523-36.
7. Rose SR, Petersen NJ, Gardner TJ, Hamill RJ, Trautner BW. Etiology of thrombocytosis in a general medicine population: analysis of 801 cases with emphasis on infectious causes. J Clin Med Res. 2012;4(6):415-23.
8. Spivak JL, Silver RT. The revised World Health Organization diagnostic criteria for polycythemia vera, essential thrombocytosis, and primary myelofibrosis: an alternative proposal. Blood. 2008;112(2):231-9.
9. Schafer AI. Thrombocytosis. N Engl J Med. 2004;350(12):1211-9.
10. Scharf RE. Drugs that affect platelet function. Semin Thromb Hemost. 2012;38(8):865-83.
11. Scharf RE. Management of bleeding in patients using antithrombotic agents: prediction, prevention, protection and problem-oriented intervention. Hamostaseologie. 2009;29(4):388-98.
12. Patrono C, Baigent C, Hirsh J, Roth G. Antiplatelet drugs: American College of Chest Physicians Evidence-Based Clinical Practice
Guidelines (8th Edition). Chest. 2008;133(6 Suppl):199s-233s.
13. Movig KL, Janssen MW, de Waal Malefijt J, Kabel PJ, Leufkens HG, Egberts AC. Relationship of serotonergic antidepressants and need for blood transfusion in orthopedic surgical patients. Arch Intern Med. 2003;163(19):2354-8.
14. Scharf RE, Rahman MM, Seidel H. The impact and management of acquired platelet dysfunction. Hamostaseologie. 2011;31(1):28-40.

