
Tóm tắt
Nội dung bài
Số lượng báo cáo nhận được từ năm 2003 đến năm 2023 được trình bày trong hình 1.
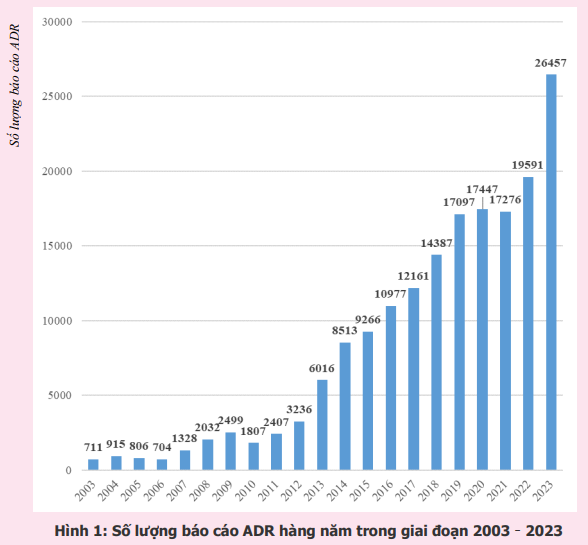
Trong số các báo cáo đã tiếp nhận, có 26137 (98,8%) báo cáo về biến cố bất lợi của thuốc, 115 (0,4%) báo cáo về chất lượng thuốc, 20 (0,1%) báo cáo về sai sót trong sử dụng thuốc và 215 (0,8%) báo cáo về các vấn đề khác (báo cáo liên quan đến thiết bị y tế, sử dụng với chỉ định chưa được phê duyệt…). Chi tiết số lượng báo cáo đã nhận được lũy tiến theo từng tháng trong năm 2023 được trình bày trong hình 2.
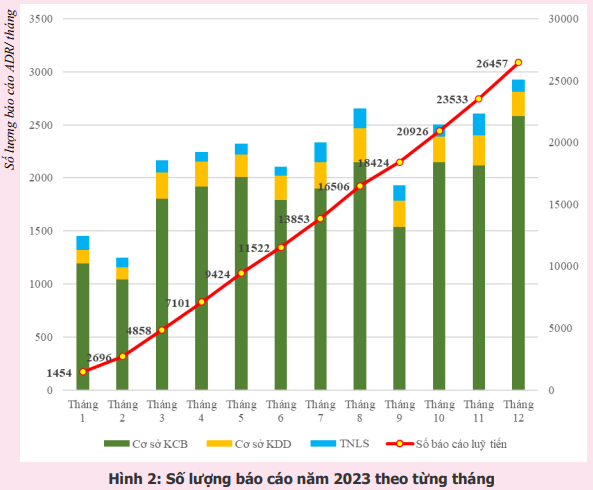
I. BÁO CÁO ADR TỪ CÁC CƠ SỞ KHÁM, CHỮA BỆNH
1. Tình hình báo cáo từ các đơn vị
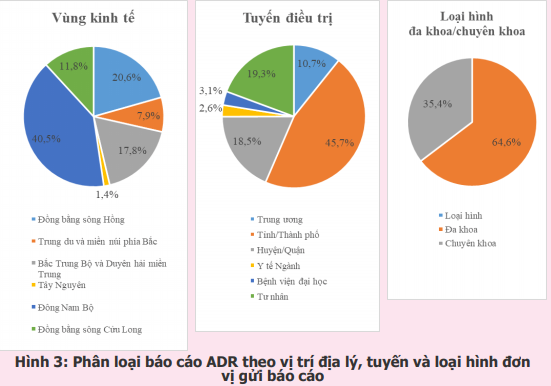
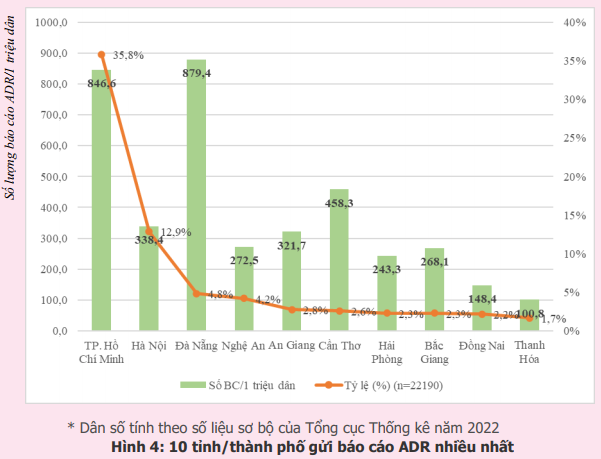
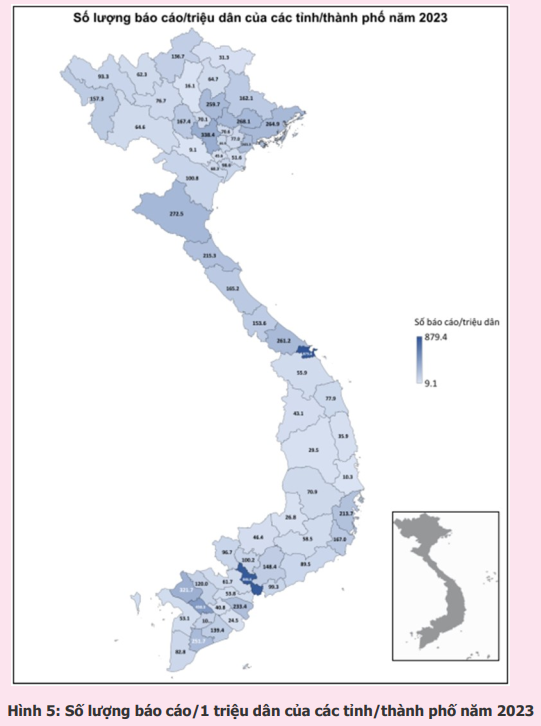
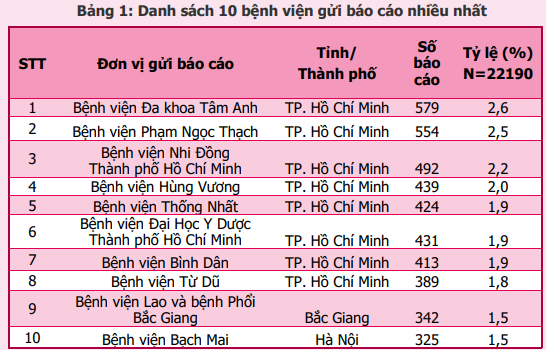
Năm 2023, 991 cơ sở khám bệnh, chữa bệnh của 63 tỉnh, thành phố trong cả nước đã gửi báo cáo ADR (tăng 17% so với năm 2022). Phần lớn báo cáo được gửi từ các đơn vị ở Đông Nam bộ và vùng đồng bằng sông Hồng, từ các bệnh viện tuyến tỉnh, bệnh viện đa khoa và bệnh viện thuộc khối các bệnh viện công lập (hình 3). Trong đó, thành phố Hồ Chí Minh và thành phố Hà Nội có tỷ lệ báo cáo cao nhất chiếm tỷ lệ tương ứng 35,8% và 12,9% tổng số báo cáo của tất cả các cơ sở khám, chữa bệnh. Các tỉnh/thành phố có số báo cáo/1 triệu dân cao hơn 200 báo cáo/1 triệu dân bao gồm thành phố Đà Nẵng, thành phố Hồ Chí Minh, thành phố Cần Thơ, thành phố Hà Nội, tỉnh An Giang, tỉnh Nghệ An, tỉnh Bắc Giang, tỉnh Quảng Ninh, tỉnh Thừa Thiên Huế, tỉnh Thái Nguyên, tỉnh Bạc Liêu, thành phố Hải Phòng, tỉnh Bến Tre, tỉnh Hà Tĩnh và tỉnh Khánh Hòa. Trong đó, thành phố Đà Nẵng là địa phương có công tác báo cáo ADR hiệu quả nhất với 879,4 báo cáo/1 triệu dân (hình 4 và hình 5). Các đơn vị có số lượng báo cáo ADR cao tập trung tại TP. Hồ Chí Minh, trong đó bệnh viện đa khoa Tâm Anh là đơn vị có số báo cáo ADR nhiều nhất trong cả nước, chiếm 2,6% tổng số báo cáo ADR từ các đơn vị khám, chữa bệnh (bảng 1).
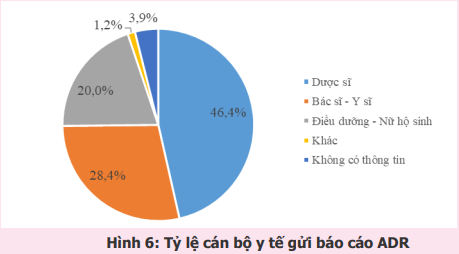
2. Các thuốc nghi ngờ gây ADR được báo cáo nhiều nhất
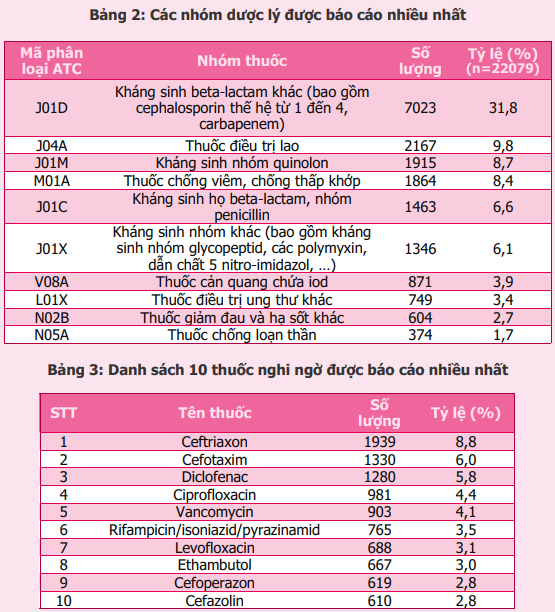
Trong 22190 báo cáo có 99 báo cáo về chất lượng thuốc và 12 báo cáo loại khác (mỹ phẩm, sữa, rượu,…), do đó thông tin về thuốc nghi ngờ được thống kê trên 22079 báo cáo, tương ứng với 17820 thuốc nghi ngờ (tỷ lệ 1,2 thuốc/1 báo cáo). Các thuốc nghi ngờ gây phản ứng có hại xuất hiện nhiều nhất trong các báo cáo ADR thuộc 3 nhóm chính: kháng sinh (ceftriaxon, cefotaxim, ciprofloxacin, vancomycin, levofloxacin, cefoperazon, cefazolin), nhóm thuốc điều trị lao (rifampicin/ isoniazid/ pyrazinamid, ethambutol) và nhóm thuốc giảm đau, hạ sốt, chống viêm (diclofenac). Ceftriaxon là thuốc nghi ngờ được báo cáo nhiều nhất với tỷ lệ 8,8%.
II. BÁO CÁO ADR TỪ CÁC ĐƠN VỊ SẢN XUẤT, KINH DOANH DƯỢC PHẨM
Trong năm 2023, 58 cơ sở kinh doanh dược đã gửi báo cáo ADR đơn lẻ, 78 đơn vị sản xuất và kinh doanh dược phẩm đã gửi báo cáo tổng hợp định kỳ (PSUR, PBRER…) và 78 cơ sở kinh doanh dược đã gửi báo cáo an toàn (2A, 2B) về Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh.
Tổng số báo cáo ADR xảy ra tại Việt Nam đã được các cơ sở kinh doanh dược ghi nhận là 2716. Trong đó, công ty Hoffmann La Roche Ltd. có số lượng báo cáo nhiều nhất (20,5%). Các thuốc nghi ngờ được báo cáo nhiều nhất từ các cơ sở kinh doanh dược thuộc 3 nhóm chính: nhóm kháng thể đơn dòng, phức hợp thuốc-kháng thể (pembrolizumab, trastuzumab, pertuzumab, bevacizumab, rituximab); nhóm ức chế protein kinase (regorafenib, lenvatinib) và thuốc cản quang (iohexol). Trong đó, regorafenib là thuốc nghi ngờ được báo cáo nhiều nhất với tỷ lệ 11,3%.
III. BÁO CÁO ADR TỪ NGHIÊN CỨU THỬ NGHIỆM LÂM SÀNG
Năm 2023, Trung tâm DI & ADR Quốc gia đã nhận được 1581 báo cáo biến cố bất lợi nghiêm trọng (giảm 19,1% so với năm 2022) xảy ra trong 74 nghiên cứu thử nghiệm lâm sàng tại Việt Nam, từ 52 đơn vị nhận thử nghiệm lâm sàng.
IV. CÁC TRƯỜNG HỢP KHẨN LIÊN QUAN ĐẾN AN TOÀN THUỐC
Trong năm 2023, Trung tâm DI & ADR Quốc gia đã xử lý 71 trường hợp phản hồi khẩn liên quan tới an toàn thuốc. Trong đó, 48 trường hợp là báo cáo ADR khẩn phản hồi cho cán bộ y tế và đơn vị gửi báo cáo ADR và 23 trường hợp công văn cung cấp thông tin về an toàn thuốc cho các cơ quan quản lý của Bộ Y tế. Trong các trường hợp báo cáo ADR khẩn, 44 trường hợp tử vong, 1 trường hợp chưa hồi phục và 5 trường hợp chuỗi báo cáo mà phản ứng có hại xảy ra với cùng một lô thuốc trong một thời gian ngắn (bao gồm các chế phẩm Amphot, Ceftriaxone 1000, Heparin Sodium Panpharma 5000 IU/ml, Nirpid 10%, vắc xin DPT-VGB-Hib (SII) và OPV). Song song với công tác phản hồi khẩn cho cá nhân, đơn vị gửi báo cáo ADR, Trung tâm DI & ADR Quốc gia cũng cập nhật các thông tin về an toàn thuốc gửi cơ quan quản lý của Bộ Y tế bao gồm:
- Tổng hợp thông tin về hiệu quả, an toàn và tình hình lưu hành của thuốc Evusheld.
- Cung cấp thông tin về nguy cơ u màng não liên quan đến các thuốc chứa progestin.
- Cung cấp thông tin liên quan đến thuốc l-ornithin l-aspartat đường tiêm.
- Cung cấp thông tin liên quan đến thuốc chứa cefoxitin.
- Rà soát lại hướng dẫn sử dụng thuốc đóng gói liều cefdinir hàm lượng 125mg và thuốc phối hợp amoxicilin/acid clavulanic hàm lượng 250mg/62,5mg.
- Cảnh báo nguy cơ rối loạn phát triển thần kinh và gây dị tật bẩm sinh ở thai nhi khi bà mẹ sử dụng topiramat trong thai kỳ.
- Cập nhật thông tin kê đơn thuốc giảm đau opioid.
- Cung cấp thông tin thống nhất cách dùng đối với thuốc chứa alpha-chymotrypsin.
- Cung cấp thông tin tình trạng cấp phép lưu hành đối với các thuốc thuộc 14 phối hợp hoạt chất bị thu hồi tại Ấn Độ.
- Cung cấp thông tin liên quan đến phản ứng có hại của thuốc Methotrexat Biddiphar 50mg/2ml, SĐK: QLĐB-638-17.
- Cảnh báo nguy cơ suy hô hấp và sốc nhiễm trùng liên quan đến Teropressin.
- Cảnh báo nguy cơ cao mắc dị tật bẩm sinh nghiêm trọng ở trẻ phơi nhiễm với hydrochloroquin trong thai kỳ.
- Cung cấp thông tin về báo cáo biến cố bát lợi liên quan đến vắn xin DPT-VGB-Hib (SII); vắc xin OPV và vắc xin IPV.
- Cung cấp thông tin về chuỗi báo cáo biến số bất lợi liên quan đến chế phẩm Heparine Sodique Panpharrmo 5000 UI/ml.
- Cung cấp thông tin liên quan đến phản ứng có hại của thuốc Nirpid 10%.
- Cập nhật nguy cơ gặp phản ứng có hại nghiêm trọng khi sử dụng thuốc chứa pseudoephedrin.
V. KẾT LUẬN VÀ ĐỀ XUẤT
Trong năm 2023, số lượng báo cáo ADR được Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh đã tiếp nhận tăng 35% so với năm 2022, tỷ lệ báo cáo vẫn chưa đồng đều giữa các địa phương, khu vực và các tuyến bệnh viện. Do đó, hoạt động báo cáo ADR cần tiếp tục được thúc đẩy hơn nữa, đặc biệt tại đơn vị, địa phương chưa tham gia báo cáo ADR. Bên cạnh các ADR rối loạn toàn thân và biểu hiện trên da, các ADR liên quan đến thuốc kháng sinh, thuốc chống lao và thuốc giảm đau, hạ sốt, chống viêm, nhân viên y tế cũng cần chú ý theo dõi, phát hiện và báo cáo các biến cố bất lợi của các nhóm thuốc khác (đặc biệt các nhóm thuốc có nguy cơ cao gây ADR, thuốc có phạm vi điều trị hẹp), các ADR trên các hệ cơ quan khác, các biến cố bất lợi cần giám sát thông qua các thăm dò chức năng chuyên sâu hay xét nghiệm cận lâm sàng.
Trong quá trình xử lý báo cáo ADR, Trung tâm nhận thấy có một số báo cáo ADR gửi từ các đơn vị và thư cảm ơn, phản hồi từ Trung tâm bị thất lạc khi gửi qua đường bưu điện. Để đảm bảo việc trao đổi thông tin được đầy đủ, kịp thời, Trung tâm xin đề nghị các đơn vị tăng cường triển khai báo cáo bằng các hình thức khác (báo cáo trực tuyến hoặc gửi thư điện tử) bên cạnh hình thức gửi qua đường bưu điện về Trung tâm. Năm 2024, Trung tâm tiếp tục duy trì gửi thư cảm ơn, phản hồi và các thông tin khác về ADR cho các đơn vị qua đường thư điện tử. Trong trường hợp có nhu cầu hoặc thay đổi cán bộ đầu mối, đề nghị các đơn vị gửi công văn tới Trung tâm DI&ADR Quốc gia, đề xuất cử 01 cán bộ đầu mối phụ trách công tác Cảnh giác Dược để nhận các thông tin nêu trên (công văn cần ghi rõ họ tên, chức vụ, đơn vị, số điện thoại và địa chỉ email của các cá nhân được đề xuất).
Trung tâm DI & ADR Quốc gia xin trân trọng cảm ơn sự hợp tác của các đơn vị và cán bộ y tế đã tham gia báo cáo ADR và mong muốn tiếp tục nhận được sự phối hợp để triển khai hiệu quả hoạt động giám sát ADR.

