
Tóm tắt
Nội dung bài
Linezolid là kháng sinh nhóm oxazolidinon, có phổ tác dụng trên các vi khuẩn Gram (+) kháng thuốc. Với sinh khả dụng đường uống xấp xỉ 100%, linezolid có thể sử dụng cả đường tiêm và đường uống. Thuốc có khả năng xâm nhập tốt vào mô (da, mô mềm, xương, cơ, mỡ, dịch lót biểu mô phế nang), không cần hiệu chỉnh liều trên bệnh nhân suy thận hay có can thiệp lọc máu nên đang ngày càng được sử dụng rộng rãi trong thực hành lâm sàng.
Giảm tiểu cầu liên quan đến linezolid là phản ứng có hại phổ biến, có thể dẫn đến cần ngừng thuốc hoặc thất bại điều trị. Thử nghiệm lâm sàng phase III của linezolid ghi nhận 2,9% bệnh nhân giảm tiểu cầu [1]. Tuy nhiên, các nghiên cứu đánh giá an toàn của linezolid giai đoạn hậu mại cho thấy tỷ lệ bệnh nhân xuất hiện giảm tiểu cầu cao hơn nhiều, dao động từ 13% đến 53%, phụ thuộc vào định nghĩa giảm tiểu cầu, tiêu chuẩn loại trừ, các yếu tố nguy cơ của bệnh nhân [2], [3], [4].
Cơ chế gây giảm tiểu cầu
Cơ chế gây giảm tiểu cầu do linezolid hiện vẫn chưa rõ ràng, liên quan đến ít nhất 2 cơ chế. Cơ chế thứ nhất là ức chế tủy xương có hồi phục dẫn đến giảm sản xuất tiểu cầu. Cơ chế này được đề xuất từ sớm, linezolid ức chế tủy xương có thể dẫn đến giảm cả hồng cầu, tiểu cầu và bạch cầu [5], [6]. Cụ thể, linezolid thúc đẩy quá trình phosphoryl hóa myosin chuỗi nhẹ 2 (MLC2) và do đó ngăn chặn quá trình giải phóng tiểu cầu từ mảnh tế bào tiểu cầu trưởng thành [5]. Cơ chế thứ hai là gây giảm tiểu cầu do miễn dịch, Bernstein và cộng sự đã đề xuất cơ chế giảm tiểu cầu do linezolid tương tự cơ chế giảm tiểu cầu qua trung gian miễn dịch gây ra bởi quinin/quinidin [7].
Thời gian khởi phát, biểu hiện lâm sàng/cận lâm sàng
Trong các nghiên cứu về an toàn thuốc ở giai đoạn hậu mại, thời gian xuất hiện giảm tiểu cầu ở bệnh nhân sử dụng linezolid rất khác nhau. Thời gian điều trị dài (≥ 7 ngày) thường làm tăng nguy cơ giảm tiểu cầu [8]. Tuy nhiên, bệnh nhân được điều trị < 7 ngày cũng có thể gặp biến cố này [8], [9].
Một số dấu hiệu và triệu chứng giảm tiểu cầu liên quan đến thuốc bao gồm [10]:
Triệu chứng toàn thân: ớn lạnh, chóng mặt, mệt mỏi, sốt, buồn nôn, nôn.
Giảm tiểu cầu mức độ trung bình (20 - 150 G/L): vết bầm tím, tiểu máu vi thể, đốm/ban xuất huyết.
Giảm tiểu cầu nghiêm trọng (< 20 G/L): xuất huyết não, chảy máu cam, ban xuất huyết, chảy máu lợi, đi tiểu ra máu, đi ngoài ra máu, rong kinh, xuất huyết sau phúc mạc.
Các yếu tố nguy cơ liên quan đến giảm tiểu cầu
- Tuổi: bệnh nhân tuổi cao (≥ 65 tuổi) có nguy cơ giảm tiểu cầu nhiều hơn [11]
- Thời gian điều trị: thời gian sử dụng linezolid kéo dài (≥ 7 ngày) làm tăng nguy cơ giảm tiểu cầu [8].
- Suy thận: Bệnh nhân suy giảm chức năng thận (Clcr < 60ml/phút) có nguy cơ gặp giảm tiểu cầu cao hơn 3,54 lần so với bệnh nhân có chức năng thận bình thường [12].
- Số lượng tiểu cầu ban đầu thấp (< 150 G/L) [8]
- Một số yếu tố nguy cơ khác được ghi nhận từ các nghiên cứu như bệnh nhân lọc máu, có bệnh lý ác tính, bilirubin toàn phần trước điều trị cao (>1,2 mg/dL) [13], [14], [15].
Theo dõi, xử trí phản ứng có hại
Tất cả bệnh nhân sử dụng linezolid cần được theo dõi công thức máu toàn phần ít nhất 1 lần/tuần. Theo dõi công thức máu toàn phần chặt chẽ hơn được khuyến cáo ở những bệnh nhân có tình trạng bệnh lý nền thiếu máu, giảm bạch cầu, giảm tiểu cầu, giảm tiểu cầu trước khi dùng thuốc; đang dùng các thuốc có thể gây giảm số lượng tế bào máu, giảm chức năng hay số lượng tiểu cầu; suy thận nặng; dùng linezolid dài hơn 10 ngày [16].
Nếu giảm tiểu cầu xảy ra ở bệnh nhân sử dụng linezolid, nên xem xét ngừng sử dụng thuốc. Trong trường hợp việc điều trị với linezolid là bắt buộc, không có lựa chọn thay thế, cần theo dõi chặt chẽ công thức máu và có chiến lược quản lý bệnh nhân phù hợp [11], [16].
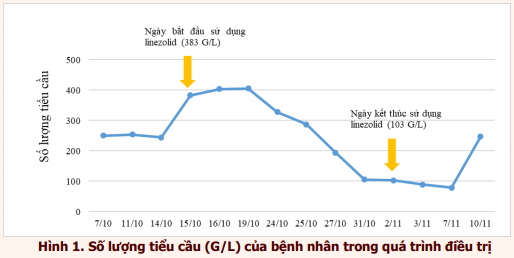
Trong tình huống lâm sàng trên, bệnh nhân có một số yếu tố nguy cơ gặp giảm tiểu cầu bao gồm tuổi cao (73 tuổi), suy thận mạn (Clcr = 8 ml/phút), thời gian điều trị dài ngày (19 ngày). Tiểu cầu bắt đầu giảm sau 10 ngày sử dụng thuốc, bệnh nhân không có dấu hiệu xuất huyết. Bệnh nhân được ngừng linezolid ở ngày 19 và theo dõi công thức máu 1-2 ngày/lần. Sau 8 ngày ngừng thuốc, số lượng tiểu cầu của bệnh nhân hồi phục dần.
Tóm lại, giảm tiểu cầu liên quan đến linezolid là phản ứng có hại phổ biến, có thể hồi phục. Tuổi cao, suy thận, sử dụng dài ngày, số lượng tiểu cầu ban đầu thấp có thể làm tăng nguy cơ giảm tiểu cầu ở bệnh nhân sử dụng linezolid. Cần theo dõi công thức máu toàn phần trong quá trình điều trị để có thể phát hiện sớm và xử trí kịp thời, đặc biệt các bệnh nhân nguy cơ cao. Trong trường hợp có giảm tiểu cầu liên quan đến linezolid, cân nhắc kỹ nguy cơ - lợi ích của việc tiếp tục điều trị và khả năng thay thế linezolid bằng kháng sinh khác.
Tài liệu tham khảo
1. Rubinstein E., Isturiz R., et al. (2003), "Worldwide assessment of linezolid's clinical safety and tolerability: comparator-controlled phase III studies", Antimicrob Agents Chemother, 47(6), pp. 1824-31.
2. Cazavet J., Bounes F. V., et al. (2020), "Risk factor analysis for linezolid-associated thrombocytopenia in critically ill patients", Eur J Clin Microbiol Infect Dis, 39(3), pp. 527-538.
3. Ichie T., Suzuki D., et al. (2015), "The association between risk factors and time of onset for thrombocytopenia in Japanese patients receiving linezolid therapy: a retrospective analysis", J Clin Pharm Ther, 40(3), pp. 279-84.
4. Thirot H., Briquet C., et al. (2021), "Clinical Use and Adverse Drug Reactions of Linezolid: A Retrospective Study in Four Belgian Hospital Centers", Antibiotics (Basel), 10(5), pp.
5. Gerson S. L., Kaplan S. L., et al. (2002), "Hematologic effects of linezolid: summary of clinical experience", Antimicrob Agents Chemother, 46(8), pp. 2723-6.
6. Tajima M., Kato Y., et al. (2016), "Linezolid-Induced Thrombocytopenia Is Caused by Suppression of Platelet Production via Phosphorylation of Myosin Light Chain 2", Biol Pharm Bull, 39(11), pp. 1846-1851.
7. Bernstein W. B., Trotta R. F., et al. (2003), "Mechanisms for linezolid-induced anemia and thrombocytopenia", Ann Pharmacother, 37(4), pp. 517-20.
8. Choi G. W., Lee J. Y., et al. (2019), "Risk factors for linezolid-induced thrombocytopenia in patients without haemato-oncologic diseases", Basic Clin Pharmacol Toxicol, 124(2), pp. 228-234.
9. Kaya Kilic E., Bulut C., et al. (2019), "Risk factors for linezolid-associated thrombocytopenia and negative effect of carbapenem combination", J Infect Dev Ctries, 13(10), pp. 886-891.
10. Kellie Jones Weddle and Patrick J. Kiel (2018), "Chapter 46: Thrombocytopenia", in Drug-induced diseases: prevention, detection, and management, pp. 1054.
11. Medicines & Healthcare products Regulatory Agency (MHRA) (2023), "Linezolid 2 mg/ml solution for infusion - Summary of product characteristics. ", pp.
12. Shi C., Xia J., et al. (2022), "Effect of renal function on the risk of thrombocytopaenia in patients receiving linezolid therapy: A systematic review and meta-analysis", Br J Clin Pharmacol, 88(2), pp. 464-475.
13. Hanai Y., Matsuo K., et al. (2016), "A retrospective study of the risk factors for linezolid-induced thrombocytopenia and anemia", J Infect Chemother, 22(8), pp. 536-42.
14. Kim H. S., Lee E., et al. (2019), "Linezolid-induced thrombocytopenia increases mortality risk in intensive care unit patients, a 10 year retrospective study", J Clin Pharm Ther, 44(1), pp. 84-90.
15. Rabon A. D., Fisher J. P., et al. (2018), "Incidence and Risk Factors for Development of Thrombocytopenia in Patients Treated With Linezolid for 7 Days or Greater", Ann Pharmacother, 52(11), pp. 1162-1164.
16. Richard H Drew PharmD, MS, FCCP, FIDP, Trisha Peel, MD, MBBS, (2023), "Linezolid and tedizolid (oxazolidinones): An overview", Uptodate, TW Post, Uptodate, Waltham, MAa, pp.

