
Tóm tắt
Nội dung bài
Trong năm 2022, Trung tâm DI & ADR Quốc gia đã ghi nhận được một số báo cáo độc tính trên thận liên quan đến vancomycin. Sau đây là một trường hợp điển hình: bệnh nhân nam, 60 tuổi, 82 kg, mắc nhiễm khuẩn viêm mô tế bào do tụ cầu vàng được chỉ định vancomycin với liều 1250 mg mỗi 12 giờ (2,5 g/ngày), từ ngày 17/10 đến ngày 20/10. Cũng trong khoảng thời gian đó, bệnh nhân được chỉ định phối hợp đồng thời piperacillin/tazobactam với liều 4,5 g x 4 lần/ngày. Chức năng thận của bệnh nhân ước tính thông qua mức lọc cầu thận (eGFR) là 91 ml/phút (ngày 17/10), sau đó đã giảm còn 35 ml/phút vào ngày 20/10. Giá trị AUC ước tính từ nồng độ vancomycin định lượng được theo phương pháp Bayes là 770 mg.h/L (vượt ngưỡng mục tiêu 400 – 600), có thể gia tăng nguy cơ gây tổn thương thận cấp liên quan đến thuốc. Theo thang phân loại RIFLE (Risk, Injury, Failure, Loss and End stage kidney diseas), bệnh nhân trên ở mức độ tổn thương thận (mức lọc cầu thận eGFR giảm > 50% so với ban đầu). Bệnh nhân đã được xử trí ngừng sử dụng vancomycin và piperacillin/tazobactam, theo dõi chức năng thận và bù dịch. Sau khi ngừng sử dụng thuốc, chức năng thận hồi phục chậm, mức lọc cầu thận 3 ngày sau đó (23/10) là 50 ml/phút.
Các nghiên cứu về độc tính trên thận liên quan đến phối hợp vancomycin và piperacillin/ tazobactam
Vancomycin là lựa chọn ưu tiên điều trị nhiễm khuẩn do tụ cầu vàng kháng methicillin (MRSA). Tuy nhiên, thuốc có nguy cơ gây tổn thương thận cấp tính (AKI) do gây viêm thận kẽ và hoại tử ống thận cấp tính [19]. Tỷ lệ xuất hiện độc tính trên thận liên quan đến vancomycin dao động từ 5% đến 43% tùy từng nghiên cứu [20]. Tỷ lệ này khác nhau giữa các nghiên cứu có thể do sự khác biệt về định nghĩa AKI được áp dụng, quần thể bệnh nhân nghiên cứu và chế độ liều vancomycin sử dụng. Bệnh nhân có thể có nhiều yếu tố nguy cơ làm tăng khả năng xuất hiện độc tính trên thận liên quan đến vancomycin như chức năng thận nền kém, bệnh mắc kèm và sử dụng đồng thời nhiều thuốc gây độc thận khác. Các thuốc có khả năng gây độc tính trên thận thường gặp bao gồm kháng sinh aminoglycosid, piperacillin/tazobactam, amphotericin B, acyclovir, các thuốc ức chế miễn dịch kháng calcineurin (tacrolimus hoặc ciclosporin) và thuốc cản quang đường tĩnh mạch [9], [14]. Trong đó, việc phối hợp vancomycin và piperacillin/tazobactam được rất nhiều nghiên cứu quan tâm, đánh giá do sự gia tăng độc tính trên thận tương đối rõ ràng. Kể từ khi được báo cáo lần đầu tiên trong y văn vào năm 2011, tổn thương thận cấp liên quan đến phối hợp vancomycin và piperacillin/tazobactam đã trở thành một vấn đề được quan tâm trong thực hành lâm sàng, với nhiều bằng chứng mới được cập nhật. Bảng 1 tóm tắt các tổng quan hệ thống về nguy cơ này, trong đó có 10/14 bài phân tích gộp dựa trên các nghiên cứu quan sát, bao gồm cả trên đối tượng bệnh nhân người lớn và bệnh nhân nhi.
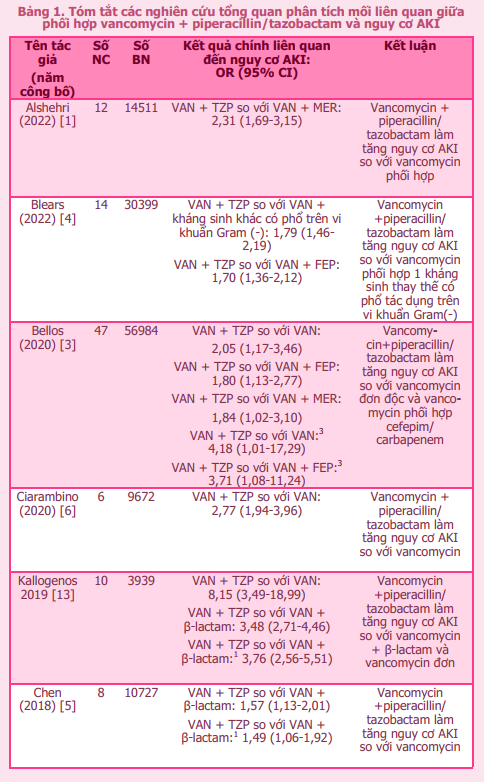
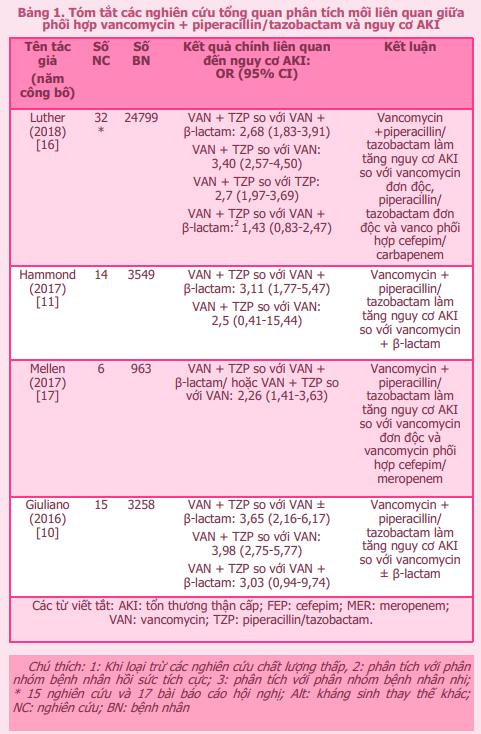
Đa số kết quả phân tích meta trên một số lượng lớn bệnh nhân cho thấy sử dụng phối hợp vancomycin + piperacillin/tazobactam làm tăng nguy cơ AKI hơn so với sử dụng vancomycin đơn độc hoặc vancomycin phối hợp với 1 kháng sinh β-lactam khác (bao gồm cefepim và carbapenem). Đáng chú ý trên bệnh nhân người lớn phối hợp vancomycin và piperacillin/tazobactam làm tăng nguy cơ AKI với tỷ số chênh (OR) từ 2 đến 3,5 lần so với sử dụng vancomycin đơn độc, trong khi đó ở bệnh nhân nhi con số này lên đến 4,18-8,15 lần [3], [13].
Cùng với các tổng quan hệ thống và phân tích meta, các phân tích hồi cứu dữ liệu với số lượng lớn bệnh nhân cũng tái khẳng định nguy cơ AKI khi phối hợp vancomycin và piperacillin/tazobactam. Một nghiên cứu hồi cứu mới đây của Komerdelj và cộng sự (2022) trên 3000 bệnh nhân người lớn có thời gian sử dụng phối hợp hai thuốc trong ít nhất 48 giờ được tiến hành trong 2 năm đã cho thấy tỷ lệ mắc AKI cao hơn đáng kể ở nhóm sử dụng vancomycin phối hợp piperacillin/tazobactam so với nhóm sử dụng phối hợp với cefepim hoặc meropenem (p < 0,001) [15]. Nghiên cứu của Downers và cộng sự (2017) phân tích hồi cứu trên 1915 bệnh nhân nhi được chỉ định sử dụng vancomycin và β-lactam tại đơn vị hồi sức tích cực cũng ghi nhận trong 157 trẻ xuất hiện tổn thương thận cấp liên quan đến kháng sinh có tới 117 trẻ được chỉ định phối hợp vancomycin và piperacillin/tazobactam. Sau khi hiệu chỉnh các yếu tố về tuổi, mức độ nặng và việc sử dụng đồng thời các tác nhân gây độc thận khác, tỷ số chênh OR giữa sử dụng phối hợp vancomycin và piperacillin/tazobactam so với phối hợp vancomycin và các β-lactam chống trực khuẩn mủ xanh khác là 3,4 (95%CI: 2,26-5,14) [8]. Nghiên cứu của Joyce và cộng sự (2019) trên 5686 trẻ điều trị tại đơn vị hồi sức tích cực cho thấy tỷ lệ mắc AKI ở giai đoạn 2 hoặc 3 (theo tiêu chuẩn KDIGO) ở nhóm sử dụng phối hợp vancomycin và piperacillin/tazobactam cao hơn đáng kể so với nhóm phối hợp vancomycin và cefepim (16,7% so với 10,6%, p = 0,02) nhưng tỷ số chênh OR đối với nguy cơ AKI không ghi nhận có ý nghĩa thống kê (OR=1,39; 95%CI 0,85-2,24) [12]. Như vậy, mặc dù chưa có nhiều các thử nghiệm lâm sàng ngẫu nhiên có đối chứng được tiến hành để làm sáng tỏ vấn đề trên, nhưng các dữ liệu hiện có từ các nghiên cứu tổng quan và nghiên cứu hồi cứu mới nhất đều cho thấy phối hợp vancomycin và piperacillin/tazobactam có nguy cơ làm tăng độc tính trên thận so với khi phối hợp vancomycin và các kháng sinh β-lactam khác.
Cơ chế xuất hiện độc tính trên thận khi phối hợp vancomycin và piperacillin/ tazobactam
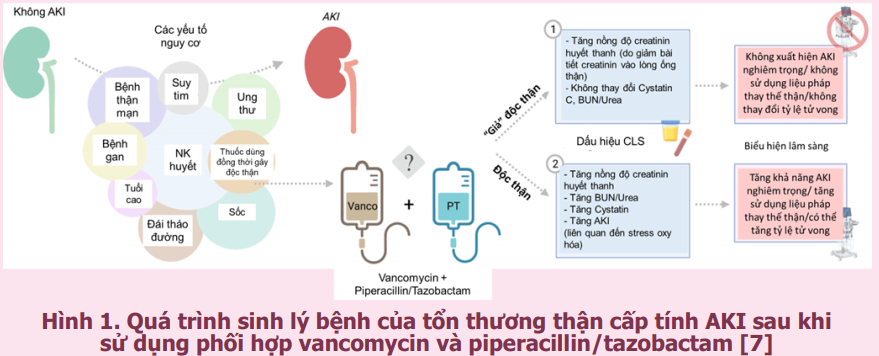
Cơ chế xuất hiện độc tính trên thận khi phối hợp vancomycin và piperacillin/ tazobactam đến nay chưa được chứng minh đầy đủ. Một trong những giả thuyết được đưa ra là piperacillin/tazobactam làm hạn chế vận chuyển creatinin vào lòng ống thận do ức chế các chất trung gian vận chuyển của nó [2]. Nghiên cứu được công bố gần đây của Miano và cộng sự (2022) đã đánh giá cụ thể nguy cơ AKI do phối hợp vancomycin và piperacillin/tazobactam có liên quan đến hiện tượng “giả” độc thận [7]. Nồng độ creatinin huyết thanh tăng trong khi các chỉ số cận lâm sàng khác (cystatin C và nitơ urê máu – BUN) không thay đổi. Kết quả nghiên cứu cũng cho thấy không gia tăng tổn thương thận cấp tính thực sự trên lâm sàng (bao gồm sử dụng liệu pháp thay thế thận hoặc tử vong) khi phối hợp hai kháng sinh này nếu sử dụng cystatin C như một chỉ số (marker) để đánh giá chức năng thận thay thế cho độ thanh thải creatinin [7]. Do đó, việc đánh giá AKI chỉ dựa trên nồng độ creatinin huyết thanh đơn thuần có thể chưa hoàn toàn chặt chẽ. Bên cạnh đó tổn thương thận có thể là hậu quả của tình trạng viêm thận kẽ dưới ngưỡng phát hiện trên lâm sàng liên quan đến piperacillin/tazobactam có thể bị khuếch đại bởi stress oxy hóa do vancomycin [2], [21]. Piperacillin/tazobactam làm giảm độ thanh thải của vancomycin dẫn đến tích lũy thuốc tại thận làm tăng khả năng độc tính. Hình 1 mô tả quá trình sinh lý bệnh của tổn thương thận cấp tính sau khi sử dụng phối hợp vancomycin và piperacillin/tazobactam.
Hướng dẫn phòng ngừa độc tính trên thận khi sử dụng vancomycin
Hiện nay chưa có các khuyến cáo chính thức từ các hướng dẫn chẩn đoán và điều trị, tuy nhiên nên tránh tối đa việc phối hợp vancomycin và piperacillin/ tazobactam. Trên các bệnh nhân có chỉ định kháng sinh chống tụ cầu vàng đang được điều trị bằng piperacillin/tazobactam, có thể cân nhắc kháng sinh thay thế cho vancomycin cũng có phổ tác dụng trên tụ cầu như linezolid hoặc daptomycin tùy theo từng loại nhiễm khuẩn và kết quả kháng sinh đồ. Linezolid là kháng sinh có hiệu quả trên các chủng vi khuẩn Gram (+) bao gồm cả Enterococci kháng vancomycin và không gây độc thận, tuy nhiên cần lưu ý thận trọng nguy cơ tương tác thuốc tiềm tàng và độc tính trên huyết học khi sử dụng thuốc kéo dài. Daptomycin cũng không gây độc thận, tuy nhiên không được chỉ định trong viêm phổi do bị bất hoạt bởi chất diện hoạt của phổi. Trên các bệnh nhân bắt buộc phải chỉ định vancomycin, cần lựa chọn kháng sinh β-lactam khác có tác dụng chống trực khuẩn mủ xanh như cefepim hoặc carbapenem thay cho piperacillin/tazobactam. Carbapenem là lựa chọn hợp lý cho bệnh nhân có nhiễm khuẩn nặng có yếu tố nguy cơ nhiễm vi khuẩn đa kháng như Enterobacteria sinh β-lactamase (ESBL), tuy nhiên cần cân nhắc sử dụng hợp lý để tránh nguy cơ gia tăng đề kháng carbapenem của các chủng Acinetobacter baumanii và Enterobacteriaceae [21].
Giám sát nồng độ thuốc trong máu (TDM) có thể đem lại lợi ích cho những trường hợp có nguy cơ cao xảy ra độc tính thận như bệnh nhân bắt buộc sử dụng đồng thời vancomycin và piperacillin/tazobactam. AUC/MIC là thông số được khuyến cáo để đánh giá cả về hiệu quả và an toàn của vancomycin. Hướng dẫn đồng thuận cập nhật về TDM vancomycin năm 2020 của các hiệp hội chuyên môn Hoa Kỳ khuyến cáo TDM vancomycin với giá trị AUC mục tiêu trong khoảng từ 400 – 600 mg.h/L (với giả định MIC = 1 mg/L) nhằm đảm bảo hiệu quả cũng như hạn chế nguy cơ độc tính trên thận. Hướng dẫn cũng khuyến cáo phương pháp ước tính AUC theo tiếp cận Bayes là cách tối ưu giúp hạn chế lấy nhiều mẫu máu và không cần đợi đến trạng thái cân bằng, từ đó phát hiện sớm nguy cơ độc thận để hiệu chỉnh liều vancomycin phù hợp cho bệnh nhân [18].
Tổng kết
Tóm lại, để giảm thiểu độc tính trên thận liên quan đến phối hợp vancomycin và piperacillin/tazobactam trong thực hành lâm sàng cần xem xét các yếu tố về phổ kháng sinh, kết quả kháng sinh đồ và dữ liệu vi sinh tại bệnh viện nhằm lựa chọn thuốc hợp lý an toàn và giảm khả năng phát sinh đề kháng thuốc. Khi sử dụng phác đồ phối hợp hai thuốc trên trong điều trị, cần giám sát chặt chẽ chức năng thận hàng ngày và lưu ý tránh tối đa phối hợp thêm các thuốc có khả năng gây độc tính trên thận khác như thuốc kháng nấm amphotericin B, thuốc ức chế miễn dịch tacrolimus, thuốc lợi tiểu quai furosemid, thuốc cản quang đường tĩnh mạch,.. Bên cạnh đó các yếu tố khác có liên quan rõ rệt đến tổn thương thận cấp do vancomycin cũng cần được chú ý bao gồm tổng liều vancomycin hàng ngày cao (> 4g/ngày), thời gian điều trị kéo dài (> 7 ngày), bệnh nhân béo phì, bệnh nhân nặng, bệnh nhân có chức năng thận nền kém [9], [14]. TDM vancomycin theo AUC là quan trọng và cần thiết để đảm bảo nồng độ thuốc trong phạm vi điều trị, nhằm phát hiện kịp thời và ngăn ngừa nguy cơ xuất hiện độc tính trên thận [18]. Việc đánh giá độc tính thận dựa trên loại chỉ số đánh giá chức năng thận nào (marker) cũng là một yếu tố cần lưu ý trong quá trình sử dụng thuốc của bệnh nhân và cần thiết phải có thêm các nghiên cứu đánh giá cụ thể cũng như liên tục cập nhật mới các bằng chứng từ y văn. Theo dõi đồng thời creatinin và cystatin C nên được xem xét để có thêm căn cứ đánh giá trong thực hành lâm sàng.
Tài liệu tham khảo
1. Alshehri A. M., Alzahrani M. Y., et al. (2022), "Comparative Risk of Acute Kidney Injury Following Concurrent Administration of Vancomycin with Piperacillin/Tazobactam or Meropenem: A Systematic Review and Meta-Analysis of Observational Studies", Antibiotics (Basel), 11(4), pp.
2. Aslan A. T., Akova M. (2022), "Piperacillin-Tazobactam Plus Vancomycin-Associated Acute Kidney Injury in Adults: Can Teicoplanin or Other Antipseudomonal Beta-Lactams Be Remedies?", Healthcare (Basel), 10(8), pp.
3. Bellos I., Karageorgiou V., et al. (2020), "Acute kidney injury following the concurrent administration of antipseudomonal beta-lactams and vancomycin: a network meta-analysis", Clin Microbiol Infect, 26(6), pp. 696-705.
4. Blears E. E., Morris J., et al. (2022), "Kidney Injury in Critically Ill Patients Treated with Vancomycin and Zosyn or an Alternative: A Systematic Review and Meta-Analysis", Surg Infect (Larchmt), 23(6), pp. 516-524.
5. Chen X. Y., Xu R. X., et al. (2018), "Acute kidney injury associated with concomitant vancomycin and piperacillin/tazobactam administration: a systematic review and meta-analysis", Int Urol Nephrol, 50(11), pp. 2019-2026.
6. Ciarambino T., Giannico O. V., et al. (2020), "Acute kidney injury and vancomycin/piperacillin/tazobactam in adult patients: a systematic review", Intern Emerg Med, 15(2), pp. 327-331.
7. Cote J. M., Kane-Gill S. L., et al. (2022), "A ray of hope in the discord: is adding piperacillin-tazobactam to vancomycin truly more nephrotoxic?", Intensive Care Med, 48(9), pp. 1208-1210.
8. Downes K. J., Cowden C., et al. (2017), "Association of Acute Kidney Injury With Concomitant Vancomycin and Piperacillin/Tazobactam Treatment Among Hospitalized Children", JAMA Pediatr, 171(12), pp. e173219.
9. Filippone E. J., Kraft W. K., et al. (2017), "The Nephrotoxicity of Vancomycin", Clin Pharmacol Ther, 102(3), pp. 459-469.
10. Giuliano C. A., Patel C. R., et al. (2016), "Is the Combination of Piperacillin-Tazobactam and Vancomycin Associated with Development of Acute Kidney Injury? A Meta-analysis", Pharmacotherapy, 36(12), pp. 1217-1228.
11. Hammond D. A., Smith M. N., et al. (2017), "Systematic Review and Meta-Analysis of Acute Kidney Injury Associated with Concomitant Vancomycin and Piperacillin/tazobactam", Clin Infect Dis, 64(5), pp. 666-674.
12. Joyce E. L., Kane-Gill S. L., et al. (2019), "Piperacillin/Tazobactam and Antibiotic-Associated Acute Kidney Injury in Critically Ill Children", J Am Soc Nephrol, 30(11), pp. 2243-2251.
13. Kalligeros M., Karageorgos S. A., et al. (2019), "The association of acute kidney injury with the concomitant use of vancomycin and piperacillin/tazobactam in children: A systematic review and meta-analysis", Antimicrob Agents Chemother, 63(12), pp.
14. Kim J. Y., Yee J., et al. (2022), "Risk factors for vancomycin-associated acute kidney injury: A systematic review and meta-analysis", Br J Clin Pharmacol, 88(9), pp. 3977-3989.
15. Komerdelj I. A., Buckley M. S., et al. (2022), "Vancomycin With Concomitant Piperacillin/Tazobactam vs. Cefepime or Meropenem Associated Acute Kidney Injury in General Ward Patients: A Multicenter Propensity Score-Matched Study", J Pharm Pract, pp. 8971900221125518.
16. Luther M. K., Timbrook T. T., et al. (2018), "Vancomycin Plus Piperacillin-Tazobactam and Acute Kidney Injury in Adults: A Systematic Review and Meta-Analysis", Crit Care Med, 46(1), pp. 12-20.
17. Mellen C. K., Ryba J. E., et al. (2017), "Does Piperacillin-Tazobactam Increase the Risk of Nephrotoxicity when Used with Vancomycin: A Meta-Analysis of Observational Trials", Curr Drug Saf, 12(1), pp. 62-66.
18. Rybak M. J., Le J., et al. (2020), "Therapeutic monitoring of vancomycin for serious methicillin-resistant Staphylococcus aureus infections: A revised consensus guideline and review by the American Society of Health-System Pharmacists, the Infectious Diseases Society of America, the Pediatric Infectious Diseases Society, and the Society of Infectious Diseases Pharmacists", Am J Health Syst Pharm, 77(11), pp. 835-864.
19. Sawada A., Kawanishi K., et al. (2018), "Biopsy-proven vancomycin-induced acute kidney injury: a case report and literature review", BMC Nephrol, 19(1), pp. 72.
20. van Hal S. J., Paterson D. L., et al. (2013), "Systematic review and meta-analysis of vancomycin-induced nephrotoxicity associated with dosing schedules that maintain troughs between 15 and 20 milligrams per liter", Antimicrob Agents Chemother, 57(2), pp. 734-44.
21. Watkins R. R., Deresinski S. (2017), "Increasing Evidence of the Nephrotoxicity of Piperacillin/Tazobactam and Vancomycin Combination Therapy-What Is the Clinician to Do?", Clin Infect Dis, 65(12), pp. 2137-2143.

