
Nội dung bài
Trong 3 tháng đầu năm 2017, Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh tiếp nhận 2340 báo cáo ADR (tăng 28,6% so với cùng kỳ năm 2016). Trong đó, 2018 báo cáo ADR được gửi từ các cơ sở khám, chữa bệnh và 344 báo cáo ADR xảy ra trên lãnh thổ Việt Nam từ các đơn vị sản xuất, kinh doanh dược phẩm (trong đó có 22 báo cáo trùng với báo cáo từ các cơ sở khám, chữa bệnh) (hình 1).
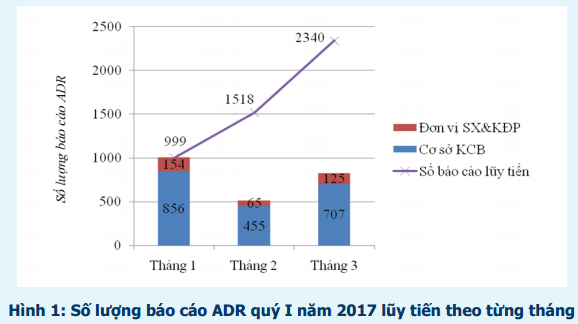
1. Báo cáo ADR từ các cơ sở khám bệnh, chữa bệnh
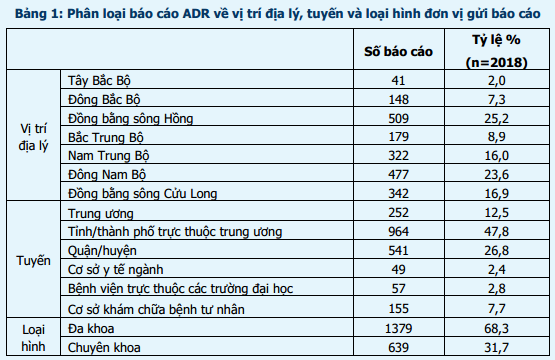
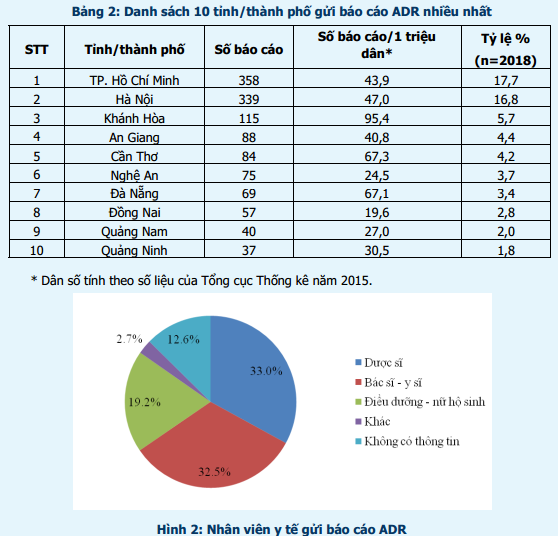
393 cơ sở khám bệnh, chữa bệnh của toàn bộ 61 tỉnh, thành phố trong cả nước đã gửi báo cáo ADR trong quý I năm 2017. Hai tỉnh chưa tham gia báo cáo ADR là Hà Giang và Phú Yên. Phần lớn báo cáo được gửi từ các đơn vị ở vùng Đông Nam bộ và đồng bằng sông Hồng, từ các bệnh viện tuyến tỉnh, bệnh viện đa khoa và bệnh viện thuộc khối công lập (bảng 1). Trong đó, thành phố Hồ Chí Minh và Hà Nội có số lượng báo cáo cao nhất (tương ứng 17,7% và 16,8% tổng số báo cáo nhận được của cả nước). Tỉnh Khánh Hòa là địa phương có công tác báo cáo ADR hiệu quả nhất với số báo cáo/1 triệu dân cao nhất trong cả nước (95,4 báo cáo/1 triệu dân) (bảng 2). Các đơn vị có số lượng báo cáo ADR cao tập trung tại TP. Hồ Chí Minh và Hà Nội. Bệnh viện Chuyên khoa Tâm thần Khánh Hòa là đơn vị có số báo cáo ADR nhiều nhất trong cả nước, chiếm 4,1% tổng số báo cáo ADR từ các đơn vị khám, chữa bệnh (bảng 3).
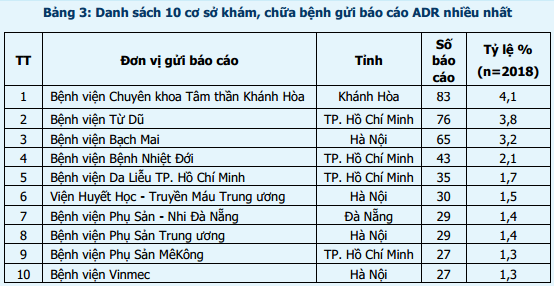
Đối tượng gửi báo cáo chủ yếu là dược sĩ (33,0%), bác sĩ - y sĩ (32,5%) và tiếp theo là điều dưỡng và nữ hộ sinh (19,2%) (hình 2).
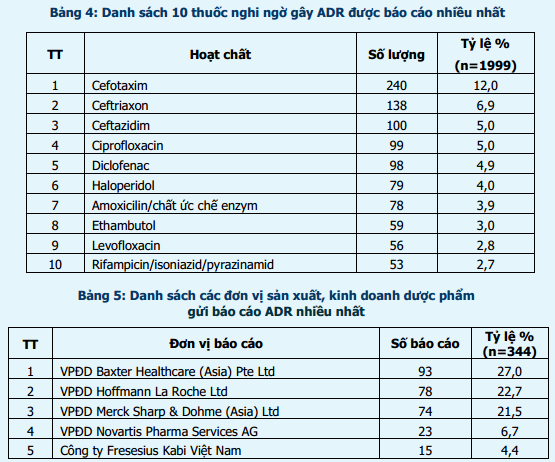
Trong số 2018 báo cáo có 19 báo cáo về các vấn đề không liên quan đến thuốc. Vì vậy, thông tin về thuốc nghi ngờ được thống kê trên 1999 báo cáo. Tổng số thuốc nghi ngờ được báo cáo là 2388 thuốc (tỷ lệ vẫn duy trì 1,2 thuốc/1 báo cáo). Các thuốc nghi ngờ gây ADR được báo cáo thuộc 4 nhóm chính: kháng sinh (cefotaxim, ceftriaxon, ceftazidim, ciprofloxacin, amoxicilin/chất ức chế enzym, levofloxacin), các thuốc điều trị lao (ethambutol và rifampicin/isoniazid/pyrazinamid), thuốc giảm đau, chống viêm (diclofenac) và thuốc chống loạn thần (haloperidol). Cefotaxim vẫn là thuốc nghi ngờ gây ra ADR được báo cáo nhiều nhất với tỷ lệ 12,0% (bảng 4).
2. Báo cáo ADR từ các đơn vị sản xuất, kinh doanh dược phẩm
Trong quý I năm 2017, 22 đơn vị sản xuất và kinh doanh dược phẩm đã gửi báo cáo ADR đơn lẻ và 33 đơn vị sản xuất và kinh doanh dược phẩm đã gửi báo cáo tổng hợp định kỳ về Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh.
Tổng số báo cáo ADR xảy ra tại Việt Nam đã được các đơn vị sản xuất, kinh doanh dược phẩm ghi nhận là 344 (trong đó có 22 báo cáo trùng với báo cáo từ các cơ sở khám, chữa bệnh), tăng 47,6% so với cùng kỳ năm 2016. Các đơn vị sản xuất, kinh doanh dược phẩm có số lượng báo cáo ADR nhiều nhất được tổng hợp trong bảng 5. Ngoài ra, các chế phẩm đang được lưu hành trên thị trường được báo cáo nhiều nhất là dung dịch thẩm phân màng bụng (27,0%), losartan (8,4%), bevacizumab (7,6%), erlotinib (4,9%), imatinib (4,9%).
3. Kết luận
Trong quý I năm 2017, số lượng báo cáo ADR được tiếp nhận đã tăng 28,6% so với cùng kỳ năm 2016, tỷ lệ báo cáo vẫn chưa đồng đều giữa các địa phương, khu vực và các tuyến bệnh viện. Do đó, công tác báo cáo và giám sát ADR cần tiếp tục được quan tâm thúc đẩy hơn nữa, đặc biệt tại đơn vị, địa phương chưa tham gia báo cáo ADR. Dược sĩ là một trong những đối tượng chính tham gia báo cáo ADR và cần tiếp tục phát huy hơn nữa vai trò của mình trong công tác đảm bảo an toàn thuốc nói chung và hoạt động theo dõi, báo cáo ADR nói riêng. Bên cạnh việc báo cáo ADR của các thuốc được sử dụng nhiều (thuốc kháng sinh, thuốc điều trị lao, thuốc giảm đau, chống viêm) và các phản ứng có hại dễ được phát hiện (dị ứng ngoài da, phản ứng phản vệ/sốc phản vệ), cán bộ y tế cần tập trung báo cáo phản ứng có hại của các thuốc mới được sử dụng tại đơn vị, phản ứng có hại mới chưa được ghi nhận và các phản ứng có hại cần xét nghiệm cận lâm sàng hoặc thăm dò chức năng chuyên biệt.
Trung tâm DI & ADR Quốc gia xin trân trọng cảm ơn sự hợp tác của các đơn vị và cán bộ y tế đã tham gia báo cáo ADR và mong muốn tiếp tục nhận được sự phối hợp để triển khai hiệu quả hoạt động giám sát ADR.

