
Tóm tắt
Nội dung bài
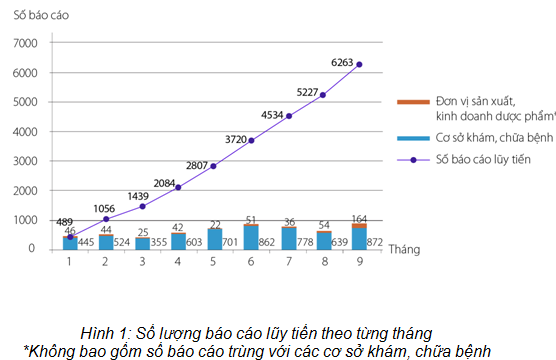
Trong 9 tháng đầu năm 2015, Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh đã tiếp nhận và xử lý 6263 báo cáo ADR, tăng 7,9% so với cùng kỳ năm 2014 (5804 báo cáo). Trong đó, 5779 báo cáo được gửi từ các cơ sở khám, chữa bệnh và 497 báo cáo ADR xảy ra trên lãnh thổ Việt Nam từ các đơn vị sản xuất, kinh doanh dược phẩm (13 báo cáo trùng với báo cáo từ các cơ sở khám, chữa bệnh). Số báo cáo nghiêm trọng là 1816 (chiếm 29,0% tổng số báo cáo). Trong số các báo cáo ADR đã tiếp nhận, có 6227 (99,5%) báo cáo về phản ứng có hại của thuốc và 31 (0,49%) báo cáo về chất lượng thuốc, 5 (0,08%) báo cáo về các vấn đề không liên quan đến thuốc. Số lượng báo cáo ADR từ Chương trình Phòng, chống HIV/AIDS là 93 (1,6%), Chương trình Chống Lao Quốc gia là 717 (12,4%) và Chương trình Phòng chống Sốt rét Quốc gia là 140 (2,5%). Đã có 3460 (55,24%) báo cáo đã được phản hồi kết quả thẩm định cho cán bộ y tế.
Chi tiết số lượng báo cáo đã nhận được lũy tiến từ tháng 1 đến tháng 9 được trình bày trong hình 1.
I. BÁO CÁO ADR TỪ CÁC CƠ SỞ KHÁM, CHỮA BỆNH
1. Tình hình báo cáo từ các đơn vị
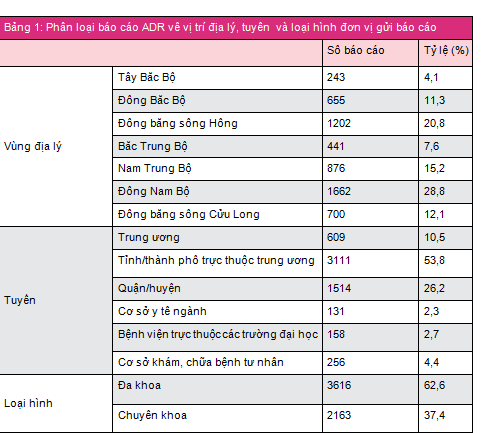
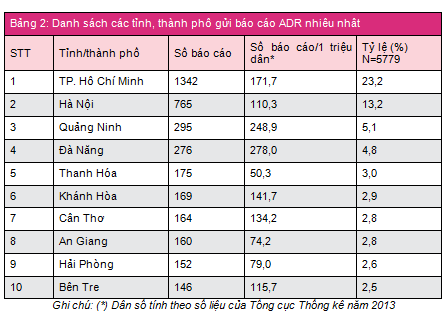
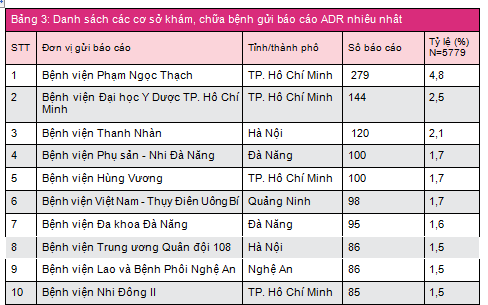
Tính đến hết 9 tháng đầu năm 2015, 614 cơ sở khám bệnh, chữa bệnh của tất cả 63 tỉnh, thành phố trong cả nước đã gửi báo cáo ADR. Phần lớn báo cáo được gửi từ các đơn vị ở vùng Đông Nam Bộ và đồng bằng sông Hồng, từ các bệnh viện tuyến tỉnh, bệnh viện đa khoa và bệnh viện thuộc khối công lập (bảng 1). TP. Hà Nội và TP. Hồ Chí Minh có số lượng báo cáo cao nhất (tương ứng 23,2% và 12,2% tổng số báo cáo nhận được của cả nước). TP. Đà Nẵng là địa phương có công tác báo cáo ADR hiệu quả nhất với số báo cáo/1 triệu dân cao nhất trong cả nước (278,0 báo cáo/1 triệu dân) (bảng 2). Các đơn vị có số lượng báo cáo ADR cao tập trung tại TP. Hồ Chí Minh, trong đó bệnh viện Phạm Ngọc Thạch là đơn vị có số báo cáo ADR nhiều nhất trong cả nước, chiếm 4,8% tổng số báo cáo ADR từ các đơn vị khám, chữa bệnh (bảng 3).
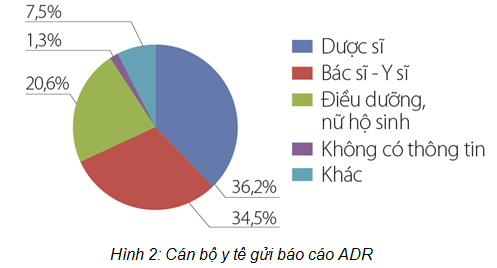
Đối tượng gửi báo cáo chủ yếu là dược sĩ (36,2%), bác sĩ - y sĩ (34,5%), tiếp theo là điều dưỡng và nữ hộ sinh (20,6%) (hình 2).
2. Các thuốc nghi ngờ gây ADR được báo cáo nhiều nhất
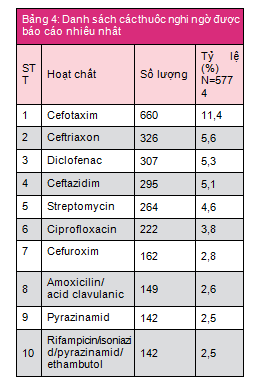
Trong số 5779 báo cáo có 5 báo cáo liên quan đến các vấn đề không liên quan đến thuốc. Vì vậy, thông tin về thuốc nghi ngờ được thống kê trên 5774 báo cáo. Tổng số thuốc nghi ngờ được báo cáo là 6975 thuốc (1,2 thuốc/1 báo cáo). Các thuốc nghi ngờ gây ADR được báo cáo thuộc 3 nhóm chính: kháng sinh (cefotaxim, ceftriaxon, ceftazidim, ciprofloxacin, cefuroxim, amoxicilin/acid clavulanic), các thuốc điều trị lao (streptomycin, pyrazinamid, dạng phối hợp rifampicin/isoniazid/pyrazinamid/ethambutol) và nhóm thuốc giảm đau, chống viêm (diclofenac). Cefotaxim vẫn là thuốc nghi ngờ gây ra ADR được báo cáo nhiều nhất với 660 báo cáo (bảng 4).
3. Các trường hợp phản hồi khẩn
Trong 9 tháng đầu năm 2015, Trung tâm DI & ADR Quốc gia đã giải quyết 58 trường hợp khẩn bao gồm 47 trường hợp báo cáo ADR khẩn phản hồi cho đơn vị gửi báo cáo ADR và 11 trường hợp công văn cung cấp thông tin về an toàn thuốc cho cơ quan quản lý của Bộ Y tế. Trong các trường hợp báo cáo ADR khẩn, có 28 trường hợp tử vong và 19 chuỗi báo cáo (thông tin về các chuỗi báo cáo ADR được cập nhật thường xuyên tại địa chỉ http://canhgiacduoc.org.vn).
II. BÁO CÁO ADR TỪ CÁC ĐƠN VỊ SẢN XUẤT, KINH DOANH DƯỢC PHẨM
Trong 9 tháng đầu năm 2015, có 24 đơn vị sản xuất, kinh doanh dược phẩm đã gửi báo cáo ADR xảy ra trên lãnh thổ Việt Nam về Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh.
Tổng số báo cáo ADR xảy ra tại Việt Nam đã được các đơn vị sản xuất, kinh doanh dược phẩm ghi nhận là 497 (trong đó có 13 báo cáo trùng với báo cáo từ các cơ sở khám, chữa bệnh). Các chế phẩm đang được lưu hành trên thị trường được báo cáo nhiều nhất là bevacizumab (63 báo cáo), imatinib (53 báo cáo), losartan (33 báo cáo), dung dịch thẩm phân màng bụng (32 báo cáo).
III. KẾT LUẬN
Trong 9 tháng đầu năm 2015, số lượng báo cáo ADR được Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh tiếp nhận tăng 7,9% so với cùng kỳ năm 2014, tỷ lệ báo cáo vẫn chưa đồng đều giữa các địa phương, khu vực và các tuyến bệnh viện. Do đó, công tác báo cáo ADR cần tiếp tục được thúc đẩy hơn nữa, đặc biệt tại đơn vị, địa phương chưa tham gia báo cáo ADR. Dược sĩ đã trở thành đối tượng chính tham gia báo cáo ADR và cần tiếp tục phát huy hơn nữa vai trò của mình trong công tác đảm bảo an toàn thuốc nói chung và hoạt động theo dõi, báo cáo ADR nói riêng. Bên cạnh việc báo cáo ADR của các thuốc được sử dụng nhiều (thuốc kháng sinh, thuốc điều trị lao, thuốc giảm đau, hạ sốt, chống viêm) và các phản ứng có hại thông thường (dị ứng ngoài da, phản ứng phản vệ/sốc phản vệ), cán bộ y tế cần tập trung báo cáo phản ứng có hại của các thuốc mới được sử dụng tại đơn vị, phản ứng có hại mới chưa được ghi nhận và các phản ứng có hại cần xét nghiệm cận lâm sàng hoặc thăm dò chức năng chuyên biệt.
Trung tâm DI & ADR Quốc gia xin trân trọng cảm ơn sự hợp tác của các đơn vị và cán bộ y tế đã tham gia báo cáo ADR và mong muốn tiếp tục nhận được sự phối hợp để triển khai hiệu quả hoạt động giám sát ADR.

