
Tóm tắt
Nội dung bài
Trong 9 tháng đầu năm 2013, Trung tâm DI & ADR Quốc gia và Trung tâm DI & ADR khu vực TP. Hồ Chí Minh đã tiếp nhận và xử lý 3875 báo cáo ADR. Trong đó, 3522 báo cáo được gửi từ các cơ sở khám, chữa bệnh, 218 báo cáo từ hoạt động Báo cáo Tự nguyện Có chủ đích (TSR) và 136 báo cáo ADR xảy ra trên lãnh thổ Việt Nam từ các đơn vị sản xuất, kinh doanh dược phẩm (có 1 báo cáo trùng giữa 1 đơn vị sản xuất, kinh doanh dược phẩm và 1 cơ sở khám, chữa bệnh). Chi tiết về số lượng báo cáo đã nhận được được trình bày trong hình 1 và hình 2.
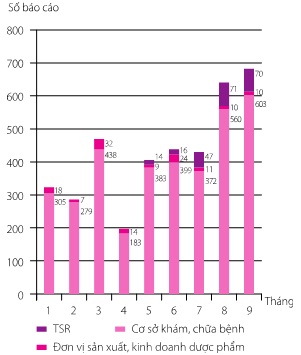
Hình 1: Số lượng báo cáo nhận được từ các nguồn trong từng tháng
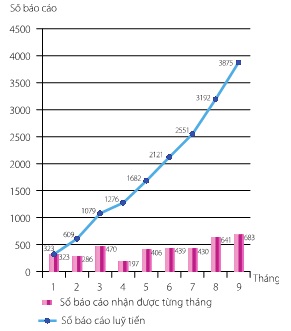
Hình 2: Số lượng báo cáo nhận được lũy tiến theo tháng
Đối tượng gửi báo cáo nhiều nhất là bác sĩ (45,09%), tiếp theo là dược sĩ (28,59%), điều dưỡng và nữ hộ sinh (18,31%) (hình 3).
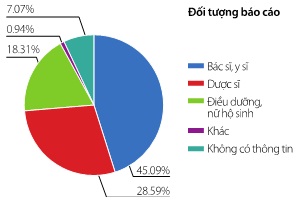
Hình 3: Tỷ lệ các đối tượng tham gia báo cáo
I. BÁO CÁO ADR TỪ CÁC CƠ SỞ KHÁM, CHỮA BỆNH
1. Tình hình báo cáo ADR từ các đơn vị
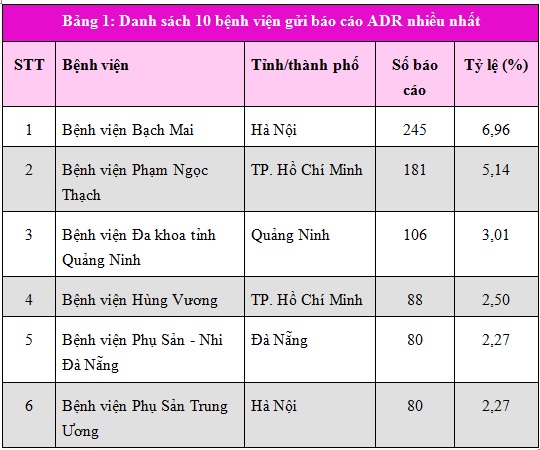
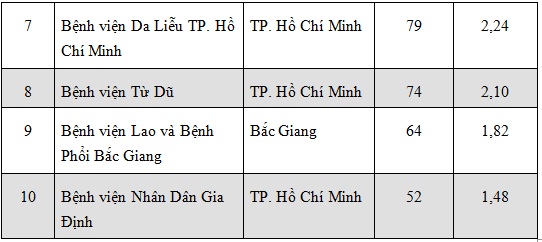
Tính đến hết quý III năm 2013, 397 cơ sở khám bệnh, chữa bệnh của 63 tỉnh, thành phố đã gửi báo cáo ADR. Danh sách 10 cơ sở khám, chữa bệnh gửi báo cáo nhiều nhất được trình bày trong bảng 1.
2. Các thuốc nghi ngờ gây ra ADR được báo cáo nhiều nhất
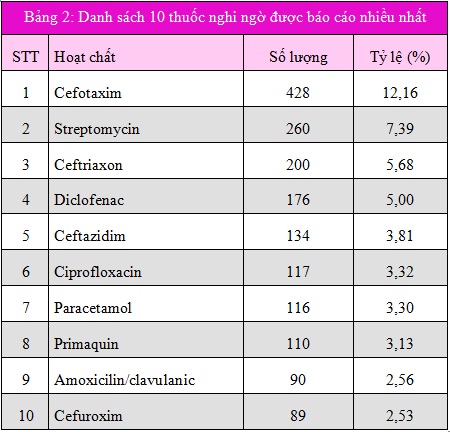
Trong 3522 báo cáo có 1 báo cáo về mỹ phẩm, 2 báo cáo về thuốc trừ sâu, do đó tổng số thuốc nghi ngờ được báo cáo được thống kê từ 3519 báo cáo là 4401 thuốc (tỷ lệ 1,25 thuốc/1 báo cáo). Các thuốc nghi ngờ gây ADR xuất hiện nhiều nhất trong các báo cáo thuộc 4 nhóm chính: nhóm thuốc kháng sinh nhiều nhất với 6 đại diện là cefotaxim, ceftriaxon, ceftazidim, ciprofloxacin, cefuroxim và amoxicilin/clavulanic; nhóm thuốc điều trị lao (streptomycin); nhóm thuốc giảm đau, hạ sốt, chống viêm (paracetamol và diclofenac) và thuốc điều trị sốt rét (primaquin). Trong đó, cefotaxim là thuốc được báo cáo nhiều nhất (12,16%) (bảng 2).
3. Các trường hợp phản hồi khẩn
Trong 3 quý đầu năm 2013, Trung tâm DI & ADR Quốc gia đã giải quyết 62 trường hợp khẩn. Trong đó, quý III có 31 trường hợp bao gồm 20 trường hợp báo cáo khẩn (tương ứng với 62 báo cáo ADR) và 11 trường hợp công văn cung cấp thông tin về an toàn thuốc cho cơ quan quản lý của Bộ Y tế. Liên quan đến các trường hợp báo cáo ADR khẩn, có 9 báo cáo tử vong (chủ yếu do sốc phản vệ) liên quan đến các thuốc: Mobic (meloxicam), Sevorane (sevofluran), suxamethonium, Sodium Chloride 0,9%, Trikazim (ceftazidim), Xenetix (iobitridol), Cefonen (ceftriaxon), Streptoken (streptokinase), vancomycin và 14 chuỗi báo cáo liên quan đến các thuốc: Propofol Lipuro 1% (propofol), NSX: B.Braun Melsungen AG, số lô: 12437033; Lidocain & Adrenalin Injection BP, NSX: Psychotropics India, số lô: 12IV-019; Ringer Lactate, NSX: Công ty Dược & Trang thiết bị Y tế Bình Định, số lô: 86GEN046, 86GEN040; Cefofast (cefotaxim), NSX: Mekophar, số lô: 11055TN; Sodium Chloride 0,9%, NSX: Anhui Double-Crane Pharmaceutical Co., Ltd., số lô: v-130483s; Hemapo (epoetin alpha), NSX: Shandong Kexing Bioproducts Co., Ltd., số lô: 201212105; Ringer Dextrose 5%, NSX: Công ty TNHH B. Braun Việt Nam, số lô: 131977741, 130337741, 130947741; Ultravist 370 (iopromid), NSX: Bayer Schering Pharma AG, số lô: T31954D; Cefotaxim, NSX: Công ty Cổ phần Dược phẩm VCP, số lô: 620613; Streptoken (streptokinase), NSX: Dongkook pharm Co., Ltd., số lô: V1332005; Cefuroxim, NSX: Công ty cổ phần dược phẩm VCP, số lô: 560613; Xenetix (iobitridol), NSX: Guerbet (France), số lô: 12WC034A; Marcain Spinal Heavy (bupivacain), NSX: AstraZeneca AB, số lô: F0075-2; Huyết thanh kháng nọc rắn hổ đất, NSX: Viện Vắc xin và Sinh phẩm Y tế (IVAC), số lô: 31.
II. BÁO CÁO ADR TỪ CÁC ĐƠN VỊ SẢN XUẤT, KINH DOANH DƯỢC PHẨM
136 báo cáo ADR xảy ra trên lãnh thổ Việt Nam được gửi từ 17 đơn vị sản xuất, kinh doanh dược phẩm đã được ghi nhận trong 9 tháng đầu năm 2013. Trong đó, 124 báo cáo ADR liên quan đến các chế phẩm đang được lưu hành trên thị trường và 12 báo cáo ADR xảy ra trên bệnh nhân trong nghiên cứu lâm sàng.
Các chế phẩm được báo cáo nhiều nhất (không bao gồm các báo cáo từ các nghiên cứu lâm sàng) là: vắc xin (32 báo cáo, trong đó 19 báo cáo liên quan đến vắc xin 5 trong 1), imatinib (18 báo cáo), peg-interferon alpha 2a (11 báo cáo), iopromid (6 báo cáo), ribavirin (6 báo cáo), rituximab (6 báo cáo). Thuốc nghi ngờ liên quan đến các trường hợp tử vong gồm: vắc xin Quinvaxem (14 báo cáo), imatinib (4 báo cáo), vắc xin bại liệt (3 báo cáo), cyclosporin (2 báo cáo), sevofluran (2 báo cáo), bisoprolol fumarat (1 báo cáo), cefuroxim (1 báo cáo), hydroxycarbamid (1 báo cáo), mycophenolat mofetil (1 báo cáo), methoxy polyethylen glycol-epoetin beta (1 báo cáo), sorafenib (1 báo cáo), vắc xin phòng papillomavirus (HPV) typ 16 và 18 ở người (1 báo cáo).
III. KẾT LUẬN
Trong 9 tháng đầu năm 2013, Trung tâm DI & ADR Quốc gia đã tiếp nhận 3875 báo cáo từ 397 cơ sở khám, chữa bệnh, 19 phòng khám ngoại trú điều trị HIV/AIDS và 17 đơn vị sản xuất, kinh doanh dược phẩm. Đối tượng thực hiện báo cáo nhiều nhất là bác sĩ, phần lớn báo cáo được gửi từ các đơn vị ở phía Nam, các bệnh viện tuyến tỉnh, bệnh viện đa khoa và bệnh viện thuộc khối công lập. Tổng số phản hồi của Trung tâm DI & ADR Quốc gia đã thực hiện trong 9 tháng đầu năm 2013 là 1563 phản hồi (40,34%). Trong đó, có 1540 phản hồi dành cho cán bộ y tế, đơn vị gửi báo cáo và 23 công văn cung cấp thông tin về an toàn thuốc cho cơ quan quản lý của Bộ Y tế.
Trung tâm DI & ADR Quốc gia xin trân trọng cảm ơn sự hợp tác của các đơn vị và cán bộ y tế đã tham gia báo cáo ADR và mong tiếp tục nhận được sự phối hợp để triển khai hiệu quả hoạt động báo cáo ADR.

